Свёртывание полипептидной цепи в нативную конформацию идёт наиболее успешно в физиологических условиях. Потеря нативной конформации, денатурация, наступает при экстремальных значениях pH, высокой температуре или под действием органических растворителей, детергентов и других денатурирующих веществ.
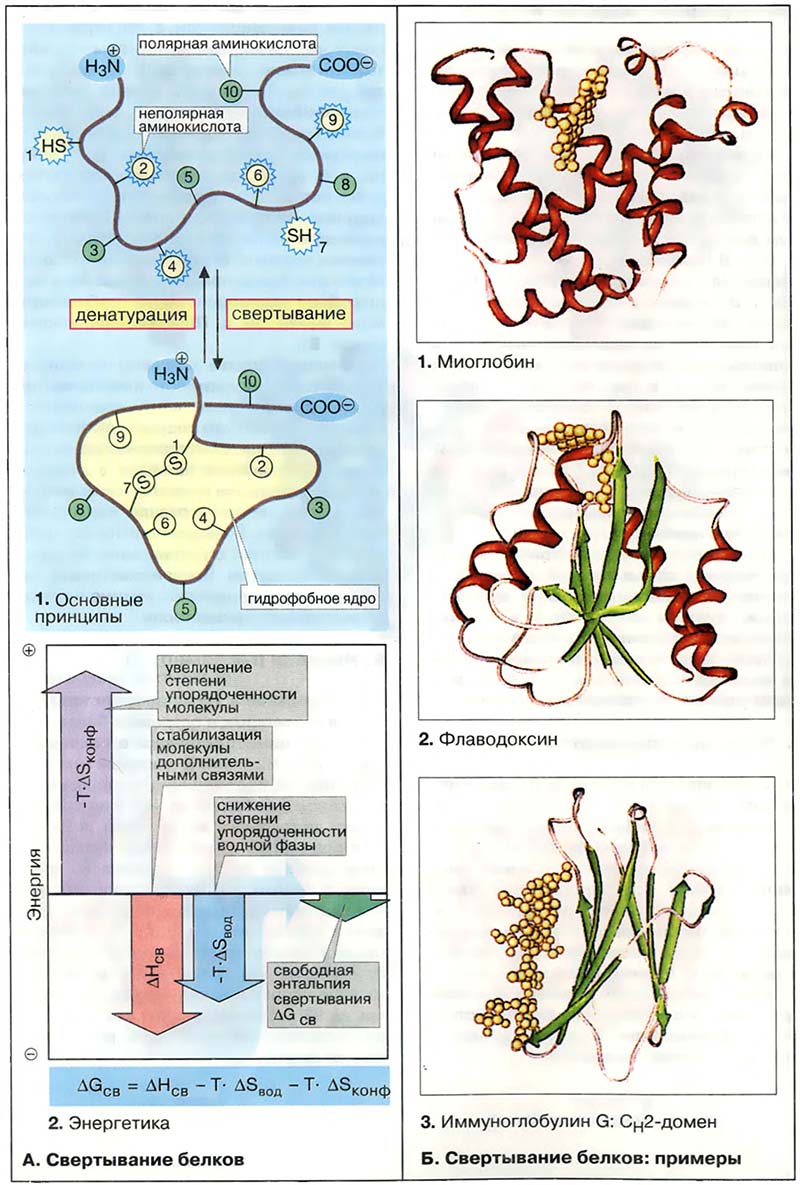
К факторам, стабилизирующим конформацию белка, относятся водородные связи, дисульфидные мостики, электростатическое взаимодействие и комплексообразование с ионами металлов (см. Метаболизм жиров). Другим очень важным стабилизирующим фактором является «гидрофобный эффект». Как отмечалось на с. Структурные белки, в смеси неполярных веществ с водой происходит разделение фаз («эффект масляных капель»), то есть идёт самопроизвольный процесс, при котором поверхность контакта между фазами стремится быть минимальной. По аналогии с этим процессом полипептидная цепь свёртывается в водной среде таким образом, чтобы как можно больше неполярных боковых групп аминокислотных остатков были бы спрятаны внутри глобулы, тогда как полярные группы контактируют с водой (1). Такой механизм позволяет объяснить распределение соответствующих группировок и в молекуле инсулина (см. Биосинтез сложных липидов).
В настоящее время не существует полного описания энергетики процесса свёртывания полипептидной цепи (2). В этом разделе обсуждается лишь предельно простая модель. В заданных условиях конформация полипептидной цепи будет устойчивой лишь в том случае, если она обладает минимумом свободной энергии (изменение свободной энергии свёртывания ΔGсв имеет знак минус) (см. Липиды). Вместе с тем свёртывание полипептидной цепи повышает степень упорядоченности белковой молекулы. А как указывалось на с. Энтальпия и энтропия, рост упорядоченности означает уменьшение энтропии системы (ΔSконф — величина отрицательная), а следовательно возрастание энтропийного члена в уравнении Гиббса—Гельмгольца (-T×ΔSконф имеет знак плюс) (фиолетовая стрелка). На процесс свёртывания также оказывают стабилизирующее воздействие ковалентные и другие типы связей, образующиеся в белковой глобуле. Поэтому изменение энтальпии свёртывания ΔHсв — величина отрицательная (красная стрелка). Другим фактором, влияющим на ход процесса, является изменение энтропии окружающей среды (воды) за счёт гидрофобного эффекта. При свёртывании полипептидной цепи снижается степень упорядоченности воды и образуется максимально возможное число водородных связей. При этом возрастает энтропия водной среды, т. е. ΔSвод — величина положительная, а следовательно, энтропийный член уравнения -Т×ΔSвод имеет знак минус (синяя стрелка). Таким образом, уменьшение энтропии полипептидной цепи перекрывается ростом энтропии окружающей среды и энтропия системы в целом возрастает. Следовательно, полипептидная цепь самопроизвольно принимает нативную конформацию, характеризующуюся минимумом свободной энергии суммарной системы (ΔGсв — величина отрицательная) (зелёная стрелка).
К факторам, стабилизирующим конформацию белка, относятся водородные связи, дисульфидные мостики, электростатическое взаимодействие и комплексообразование с ионами металлов (см. Метаболизм жиров). Другим очень важным стабилизирующим фактором является «гидрофобный эффект». Как отмечалось на с. Структурные белки, в смеси неполярных веществ с водой происходит разделение фаз («эффект масляных капель»), то есть идёт самопроизвольный процесс, при котором поверхность контакта между фазами стремится быть минимальной. По аналогии с этим процессом полипептидная цепь свёртывается в водной среде таким образом, чтобы как можно больше неполярных боковых групп аминокислотных остатков были бы спрятаны внутри глобулы, тогда как полярные группы контактируют с водой (1). Такой механизм позволяет объяснить распределение соответствующих группировок и в молекуле инсулина (см. Биосинтез сложных липидов).
В настоящее время не существует полного описания энергетики процесса свёртывания полипептидной цепи (2). В этом разделе обсуждается лишь предельно простая модель. В заданных условиях конформация полипептидной цепи будет устойчивой лишь в том случае, если она обладает минимумом свободной энергии (изменение свободной энергии свёртывания ΔGсв имеет знак минус) (см. Липиды). Вместе с тем свёртывание полипептидной цепи повышает степень упорядоченности белковой молекулы. А как указывалось на с. Энтальпия и энтропия, рост упорядоченности означает уменьшение энтропии системы (ΔSконф — величина отрицательная), а следовательно возрастание энтропийного члена в уравнении Гиббса—Гельмгольца (-T×ΔSконф имеет знак плюс) (фиолетовая стрелка). На процесс свёртывания также оказывают стабилизирующее воздействие ковалентные и другие типы связей, образующиеся в белковой глобуле. Поэтому изменение энтальпии свёртывания ΔHсв — величина отрицательная (красная стрелка). Другим фактором, влияющим на ход процесса, является изменение энтропии окружающей среды (воды) за счёт гидрофобного эффекта. При свёртывании полипептидной цепи снижается степень упорядоченности воды и образуется максимально возможное число водородных связей. При этом возрастает энтропия водной среды, т. е. ΔSвод — величина положительная, а следовательно, энтропийный член уравнения -Т×ΔSвод имеет знак минус (синяя стрелка). Таким образом, уменьшение энтропии полипептидной цепи перекрывается ростом энтропии окружающей среды и энтропия системы в целом возрастает. Следовательно, полипептидная цепь самопроизвольно принимает нативную конформацию, характеризующуюся минимумом свободной энергии суммарной системы (ΔGсв — величина отрицательная) (зелёная стрелка).
Статьи раздела «Свёртывание белков»:
- Свёртывание белков
- А. Свёртывание белков
- Б. Свёртывание белков: примеры
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
В книге собраны лучшие из современных методов выделения и анализа важнейшего ...
 Geobiology: Objectives, Concepts, Perspectives, First Edition
Geobiology: Objectives, Concepts, Perspectives, First Edition Book DescriptionGeobiology is an exciting and rapidly developing research discipline that opens new perspectives in understanding Earth as a system. ...
 Cell Biology: With STUDENT CONSULT Online Access
Cell Biology: With STUDENT CONSULT Online Access A masterful, richly illustrated introduction to the cell biology that you need to know.
 Introductory Chemistry: Concepts and Critical Thinking (6th Edition)
Introductory Chemistry: Concepts and Critical Thinking (6th Edition) Introductory Chemistry: Concepts and Critical Thinking, Sixth Edition is a comprehensive learning system that offers print and media resources as well ...