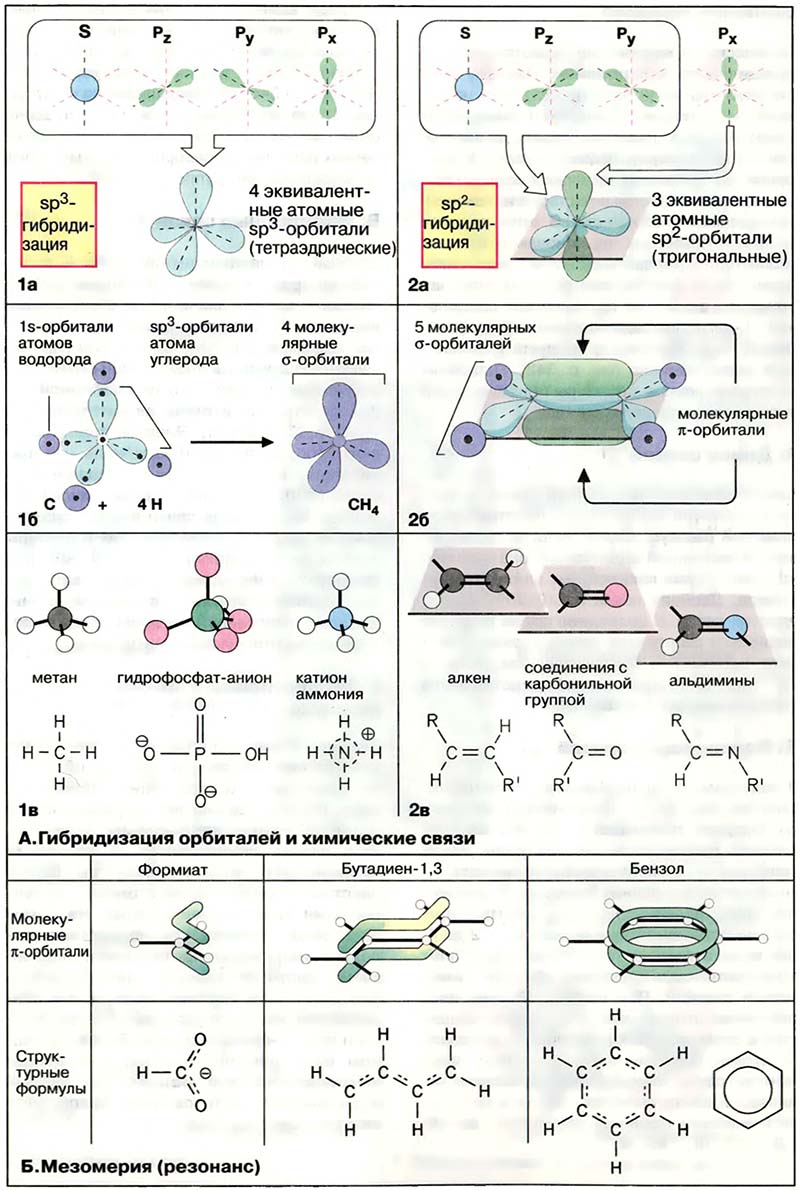
Большинство биомолекул — соединения углерода с водородом, кислородом, азотом, серой или фосфором. Устойчивые ковалентные связи между этими атомами неметаллов образуются в результате перекрывания определённых орбиталей двух атомов и формирования молекулярных орбиталей (см. Кинетика химических реакций), на которых располагаются по одному электрону от каждого атома. Так, четыре валентных электрона атома углерода занимают атомные орбитали 2s и 2р (1а). 2s-Орбиталь имеет форму шара (шаровую симметрию), а три 2p-орбитали — форму гантелей, вытянутых вдоль осей х, у, z. Следовало ожидать, что атомы углерода будут образовывать по крайней мере две различные молекулярные орбитали. Однако в действительности все четыре связи эквивалентны за счёт гибридизации орбиталей. Благодаря суммированию энергий одной s- и трёх р-орбиталей атом углерода образует четыре равноценные sp3-атомные орбитали, направленные по осям тетраэдра (sp3-гибридизация). Перекрывание таких орбиталей с 1s-орбиталями атомов водорода приводит к образованию четырёх σ-молекулярных орбиталей (1б). Это означает, что валентность атома углерода равна четырём, а в молекуле метана (CH4) имеются четыре простые (одинарные) ковалентные связи. По такому же принципу образуются простые связи между другими атомами. Так, фосфат-анион и катион аммония также имеют тетраэдрическую форму (1в).
Часто встречается тип связи, образованной за счёт гибридизации 2s-орбитали только с двумя из трёх 2p-орбиталей (sp2-гибридизация, 2а). В результате формируются три эквивалентные гибридные sp2-орбитали, расположенные в одной плоскости под углом 120°. Оставшаяся 2px-орбиталь располагается перпендикулярно плоскости. При формировании молекулярных орбиталей такие атомы могут образовывать два различных типа связей (2б): три sp2-орбитали образуют σ-связи, как описано выше, а электроны двух 2pх-орбиталей от двух атомов, то есть π-электроны, — вытянутую молекулярную π-орбиталь над и под плоскостью, занимаемой σ-связями. Этот тип связи носит название двойной связи. Двойные связи состоят из одной σ- и одной π-связей. Такой тип связи образуется лишь при наличии sp2-гибридизации у двух атомов, принимающих участие в её образовании. В отличие от простой связи вращение вокруг двойных связей невозможно, поскольку это должно вызывать разрушение π-орбиталей. Поэтому атомы при двойной связи лежат в одной плоскости (2в), что в свою очередь делает возможным существование цис- и транс-изомеров (см. Изомерия).
Часто встречается тип связи, образованной за счёт гибридизации 2s-орбитали только с двумя из трёх 2p-орбиталей (sp2-гибридизация, 2а). В результате формируются три эквивалентные гибридные sp2-орбитали, расположенные в одной плоскости под углом 120°. Оставшаяся 2px-орбиталь располагается перпендикулярно плоскости. При формировании молекулярных орбиталей такие атомы могут образовывать два различных типа связей (2б): три sp2-орбитали образуют σ-связи, как описано выше, а электроны двух 2pх-орбиталей от двух атомов, то есть π-электроны, — вытянутую молекулярную π-орбиталь над и под плоскостью, занимаемой σ-связями. Этот тип связи носит название двойной связи. Двойные связи состоят из одной σ- и одной π-связей. Такой тип связи образуется лишь при наличии sp2-гибридизации у двух атомов, принимающих участие в её образовании. В отличие от простой связи вращение вокруг двойных связей невозможно, поскольку это должно вызывать разрушение π-орбиталей. Поэтому атомы при двойной связи лежат в одной плоскости (2в), что в свою очередь делает возможным существование цис- и транс-изомеров (см. Изомерия).
Статьи раздела «Химические связи»:
- А. Гибридизация орбиталей и химические связи
- Б. Мезомерия (резонанс)
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
Книга известного английского биохимика посвящена хемиосмотической теории, ...
В монографии д.б.н., в.н.с. ИБК РАН Н.Л.Векшина на примере актиномицинов ...
 NMR Studies of Structural Motifs: Protein Folding and Ligand Binding
NMR Studies of Structural Motifs: Protein Folding and Ligand Binding NMR of Structural Motifs: The agrin G3 domain is critical in development and maintenance of the neuromuscular junction. G3 binds -dystroglycan and ...
 Солитоны в молекулярных системах
Солитоны в молекулярных системах В монографии изложены новейшие подходы к изучению транспорта энергии и ...