Большая часть потребляемого в цитратном цикле ацетил-КоА получает ацетильные остатки, образовавшиеся в результате β-окисления жирных кислот (см. Потенциал покоя и потенциал действия) и окислительного декарбоксилирования пирувата, катализируемого пируватдегидрогеназой (см. Кислотно-основной баланс). Оба процесса протекают в матриксе митохондрий.
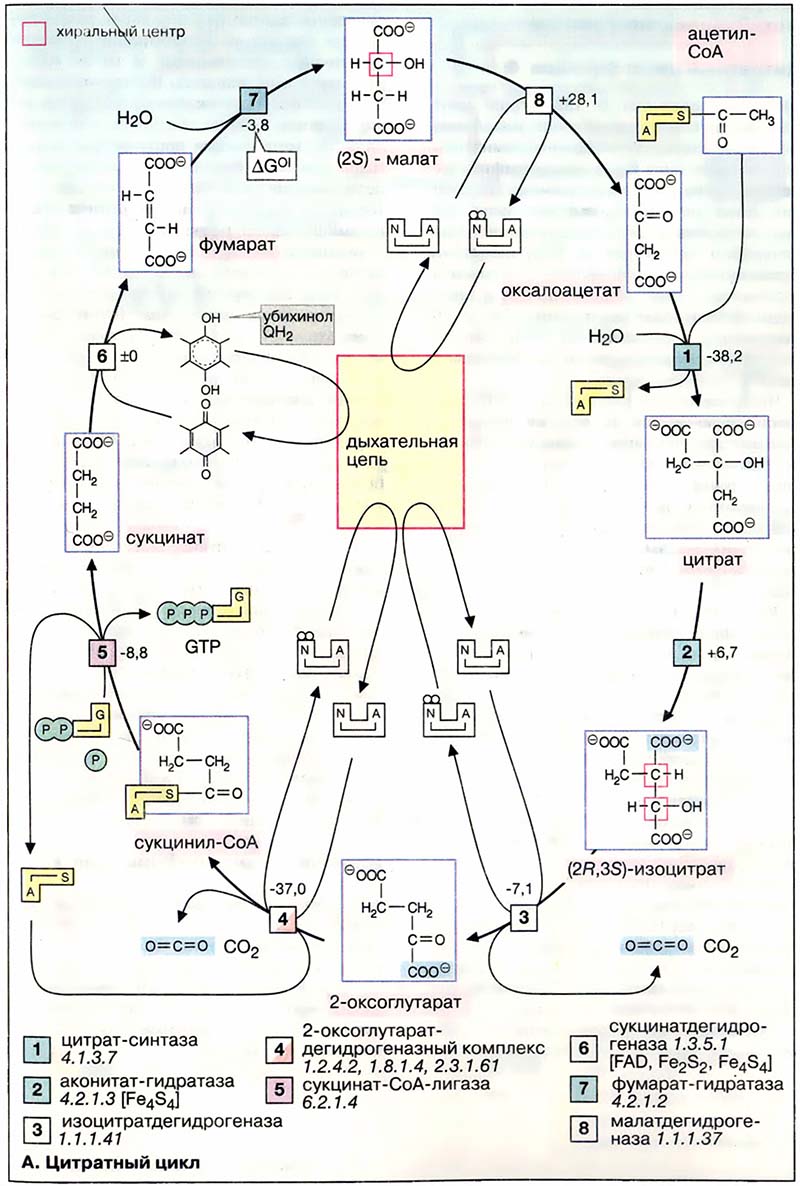
Окисление ацетильных остатков включает ряд промежуточных стадий, образующих цикл: сначала ацетильная группа в реакции, катализируемой цитрат-синтазой [1], конденсируется с молекулой оксалоацетата с образованием цитрата (цикл получил своё название по продукту этой реакции). На следующей стадии [2] цитрат изомеризуется в изоцитрат с переносом гидроксильной группы внутри молекулы. При этом промежуточный продукт реакции, ненасыщенный аконитат, остаётся во время реакции связанным с ферментом (на схеме не показано). Поэтому фермент, катализирующий реакцию, называют аконитат-гидратазой [2] («аконитазой»).
Свойства аконитат-гидратазы обеспечивают абсолютную стереоспецифичность изомеризации. В то время как цитрат не обладает хиральностью, изоцитрат содержит два асимметрических центра и может существовать в четырёх изомерных формах. Однако в цитратном цикле образуется только один из стереоизомеров, (2R,3S)-изоцитрат (см. Углеводы).
На следующей стадии изоцитратдегидрогеназа (3) окисляет гидроксигруппу изоцитрата в оксогруппу с одновременным отщеплением одной из карбоксильных групп в виде CO2 и образованием 2-оксоглутарата. Последующее образование сукцинил-КоА [4], включающее реакции окисления и декарбоксилирования, катализируется мультиферментным комплексом, 2-оксоглутаратдегидрогеназой (дегидрогеназы кетокислот рассмотрены на предыдущей странице). Расщепление тиолсложноэфирной связи сукцинил-КоА с образованием сукцината и кофермента А, катализируемое сукцинат-КоА-лигазой [«тиокиназой» (5)], — высокоэкзоэргическая реакция, энергия которой используется для синтеза фосфоангидридной связи («субстратного фосфорилирования», см. Пищеварение: общие сведения). В цитратном цикле синтезируется не АТФ, как в большинстве таких реакций, а гуанозинтрифосфат [ГТФ (GTP)], который легко превращается в АТФ нуклеозиддифосфаткиназой (на схеме не показано).
В приведённых реакциях ацетильный остаток полностью окисляется до CO2. Однако одновременно молекула переносчика оксалоацетата восстанавливается в сукцинат. В трёх последующих реакциях цикла сукцинат снова превращается в оксалоацетат. Вначале сукцинатдегидрогеназа [6] окисляет сукцинат в фумарат. В отличие от других ферментов цикла сукцинатдегидрогеназа является интегральным белком внутренней митохондриальной мембраны. Поэтому её относят также к комплексу II дыхательной цепи. Сукцинатдегидрогеназа содержит ФАД (FAD) в качестве простетической группы, однако фактическим акцептором электронов является убихинон. Затем к двойной связи фумарата с помощью фумарат-гидратазы («фумаразы», [7]) присоединяется вода и образуется хиральный (2S)-малат. На последней стадии цикла малат окисляется малатдегидрогеназой [8] в оксалоацетат с образованием НАДН + Н+. Эта реакция замыкает цитратный цикл.
Общий баланс цитратного цикла состоит в том, что из одного ацетильного остатка образуются 2 CO2, 3 НАДН + Н+ и одна молекула восстановленного убихинона (QH2). При этом за счёт восстановленных форм коферментов путём окислительного фосфорилирования в клетке синтезируются 9, а с учётом трансформации одной молекулы ГТФ — 10 молекул АТФ (см. Дыхание и брожение).
Окисление ацетильных остатков включает ряд промежуточных стадий, образующих цикл: сначала ацетильная группа в реакции, катализируемой цитрат-синтазой [1], конденсируется с молекулой оксалоацетата с образованием цитрата (цикл получил своё название по продукту этой реакции). На следующей стадии [2] цитрат изомеризуется в изоцитрат с переносом гидроксильной группы внутри молекулы. При этом промежуточный продукт реакции, ненасыщенный аконитат, остаётся во время реакции связанным с ферментом (на схеме не показано). Поэтому фермент, катализирующий реакцию, называют аконитат-гидратазой [2] («аконитазой»).
Свойства аконитат-гидратазы обеспечивают абсолютную стереоспецифичность изомеризации. В то время как цитрат не обладает хиральностью, изоцитрат содержит два асимметрических центра и может существовать в четырёх изомерных формах. Однако в цитратном цикле образуется только один из стереоизомеров, (2R,3S)-изоцитрат (см. Углеводы).
На следующей стадии изоцитратдегидрогеназа (3) окисляет гидроксигруппу изоцитрата в оксогруппу с одновременным отщеплением одной из карбоксильных групп в виде CO2 и образованием 2-оксоглутарата. Последующее образование сукцинил-КоА [4], включающее реакции окисления и декарбоксилирования, катализируется мультиферментным комплексом, 2-оксоглутаратдегидрогеназой (дегидрогеназы кетокислот рассмотрены на предыдущей странице). Расщепление тиолсложноэфирной связи сукцинил-КоА с образованием сукцината и кофермента А, катализируемое сукцинат-КоА-лигазой [«тиокиназой» (5)], — высокоэкзоэргическая реакция, энергия которой используется для синтеза фосфоангидридной связи («субстратного фосфорилирования», см. Пищеварение: общие сведения). В цитратном цикле синтезируется не АТФ, как в большинстве таких реакций, а гуанозинтрифосфат [ГТФ (GTP)], который легко превращается в АТФ нуклеозиддифосфаткиназой (на схеме не показано).
В приведённых реакциях ацетильный остаток полностью окисляется до CO2. Однако одновременно молекула переносчика оксалоацетата восстанавливается в сукцинат. В трёх последующих реакциях цикла сукцинат снова превращается в оксалоацетат. Вначале сукцинатдегидрогеназа [6] окисляет сукцинат в фумарат. В отличие от других ферментов цикла сукцинатдегидрогеназа является интегральным белком внутренней митохондриальной мембраны. Поэтому её относят также к комплексу II дыхательной цепи. Сукцинатдегидрогеназа содержит ФАД (FAD) в качестве простетической группы, однако фактическим акцептором электронов является убихинон. Затем к двойной связи фумарата с помощью фумарат-гидратазы («фумаразы», [7]) присоединяется вода и образуется хиральный (2S)-малат. На последней стадии цикла малат окисляется малатдегидрогеназой [8] в оксалоацетат с образованием НАДН + Н+. Эта реакция замыкает цитратный цикл.
Общий баланс цитратного цикла состоит в том, что из одного ацетильного остатка образуются 2 CO2, 3 НАДН + Н+ и одна молекула восстановленного убихинона (QH2). При этом за счёт восстановленных форм коферментов путём окислительного фосфорилирования в клетке синтезируются 9, а с учётом трансформации одной молекулы ГТФ — 10 молекул АТФ (см. Дыхание и брожение).
Статьи раздела «Цитратный цикл: реакции»:
- Цитратный цикл: реакции
- А. Цитратный цикл
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Молекулярное моделирование. Теория и практика
Молекулярное моделирование. Теория и практика В научном издании, написанном учёными из Германии, Франции и Швейцарии, имеющими ...
 Biotechnology Annual R Volume 14 (Biotechnology Annual Review) (Biotechnology Annual Review)
Biotechnology Annual R Volume 14 (Biotechnology Annual Review) (Biotechnology Annual Review) Biotechnology is a diverse, complex, and rapidly evolving field. Students and experienced researchers alike face the challenges of staying on top of ...
 The Reef Aquarium: Science, Art, and Technology, Vol. 3
The Reef Aquarium: Science, Art, and Technology, Vol. 3 The Reef Aquarium Volume Three: Science, Art, and Technology Reefkeeping science involves the interplay of biology, chemistry, and physics. However, a ...
 Анализ биологических последовательностей
Анализ биологических последовательностей Предлагаемая книга отражает современное состояние сравнительно новой, но весьма ...