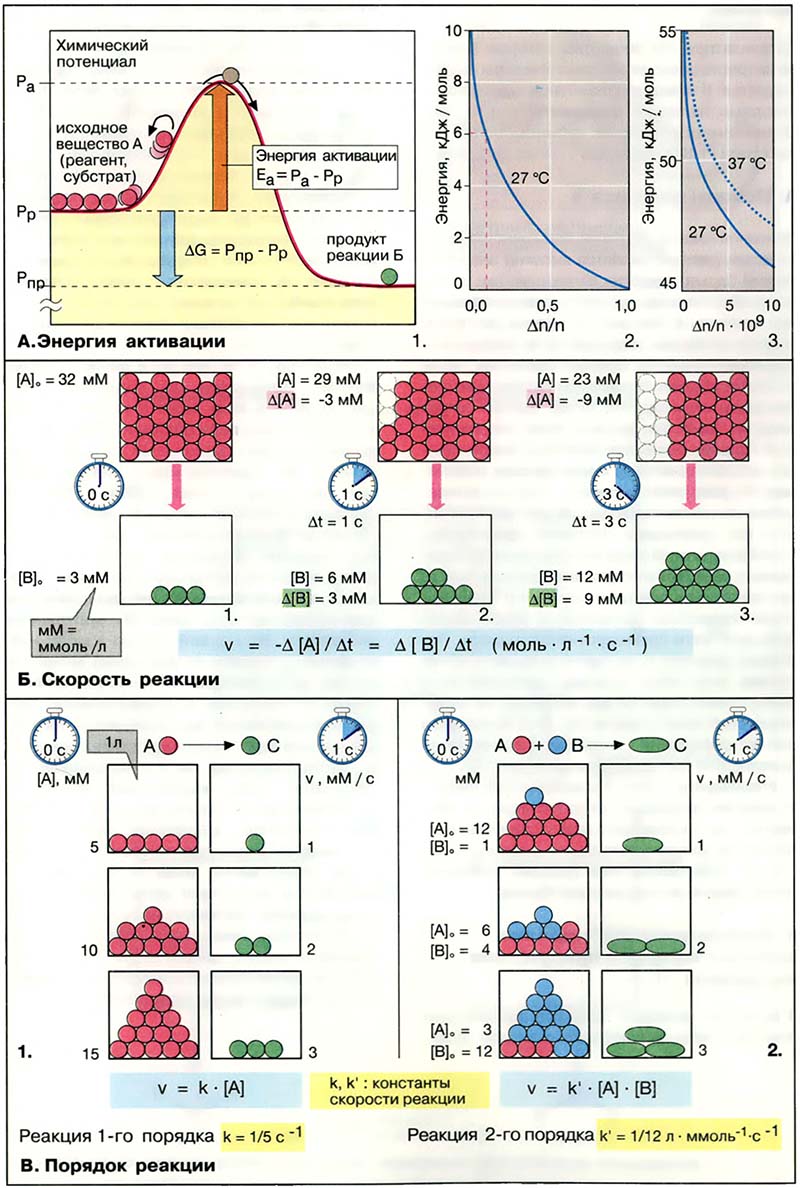
Скорость реакции зависит не только от энергии активации и температуры, но и от концентрации реагентов. Если имеется лишь один субстрат A (1), то скорость v прямо пропорциональна концентрации [A]; это реакция первого порядка. Если в реакции участвуют два реагента A и B (2), то речь идёт о реакции второго порядка . В таком случае v пропорциональна произведению концентрации реагентов. Коэффициенты k и k’ — константы скорости реакции — зависят от типа реакции и условий её проведения.
На схеме Б приведена кинетика простых необратимых реакций. Обратимые или многоступенчатые реакции могут быть разделены на промежуточные реакции первого или второго порядка и описаны с помощью соответствующих уравнений (см. кинетика Михаэлиса-Ментен, с. Кинетика ферментативных реакций).
На схеме Б приведена кинетика простых необратимых реакций. Обратимые или многоступенчатые реакции могут быть разделены на промежуточные реакции первого или второго порядка и описаны с помощью соответствующих уравнений (см. кинетика Михаэлиса-Ментен, с. Кинетика ферментативных реакций).
Статьи раздела «Кинетика химических реакций»:
- Кинетика химических реакций
- А. Энергия активации
- Б. Скорость реакции
- В. Порядок реакции
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Кинетика и термодинамика биохимических процессов
Кинетика и термодинамика биохимических процессов В книге систематически излагаются вопросы применения кинетики и термодинамики к ...
 Новейшие методы исследования биосистем
Новейшие методы исследования биосистем Книга охватывает широкий круг методов, таких как молекулярная динамика, ...
 Физика белка. Курс лекций с цветными и стереоскопическими иллюстрациями и задачами
Физика белка. Курс лекций с цветными и стереоскопическими иллюстрациями и задачами Физика белка простирается от классификации и принципов устройства белков ...
 Микроэлементы в окружающей среде. Биогеохимия, биотехнология и биоремедиация
Микроэлементы в окружающей среде. Биогеохимия, биотехнология и биоремедиация Книга посвящена анализу роли микроэлементов (металлов и металлоидов) в ...