Скорость химической реакции определяют по изменению концентрации одного из реагентов или продуктов реакции за определённый период времени. В приведённом примере в 1 л раствора за 1 с расходуется 3 ммоля реагента и, в результате образуется 3 ммоля продукта. Это соответствует скорости реакции
v = 3 мМ×с-1 = 3×10-3 моль×л-1×с-1
v = 3 мМ×с-1 = 3×10-3 моль×л-1×с-1
Статьи раздела «Кинетика химических реакций»:
- Кинетика химических реакций
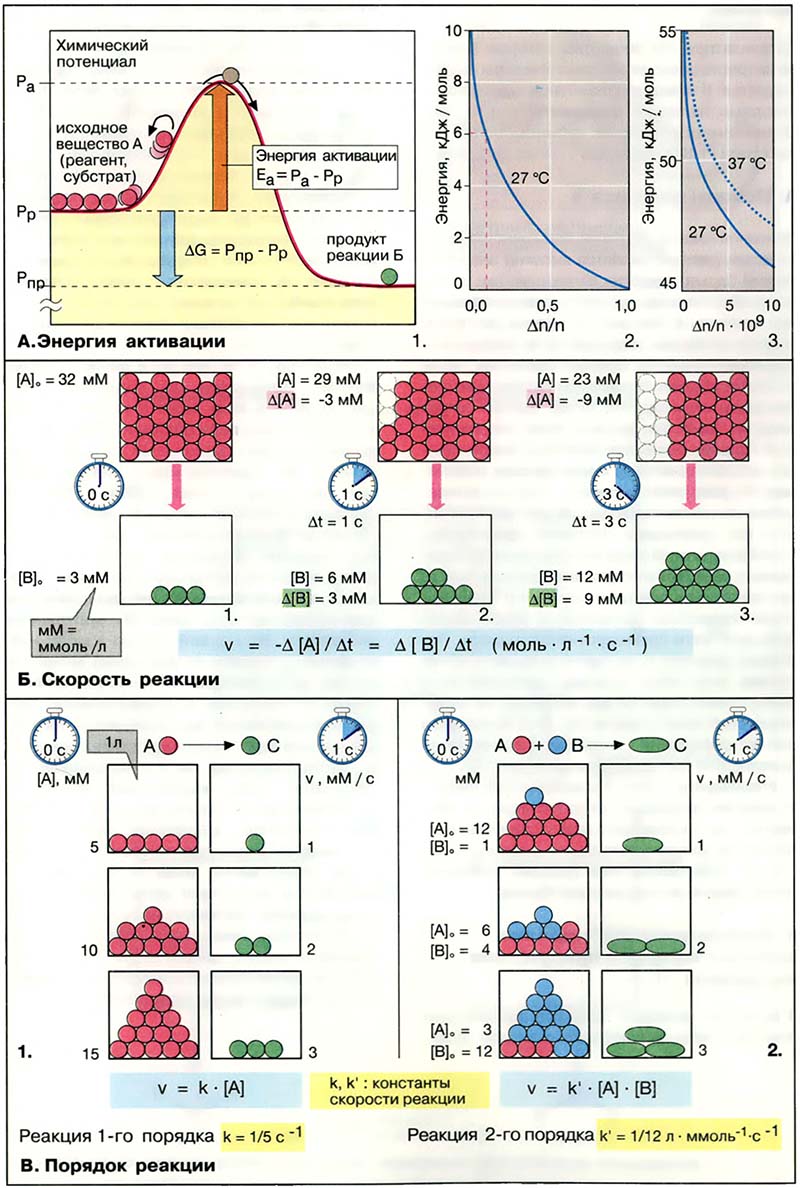
- А. Энергия активации
- Б. Скорость реакции
- В. Порядок реакции
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
Монография посвящена математическому моделированию и исследованию нелинейных ...
 Биокатализ и биокатализаторы. Исторический очерк
Биокатализ и биокатализаторы. Исторический очерк Книга посвящена истории возникновения и развития двух основных проблем ...
В книге даётся богатейший, хорошо систематизированный справочный материал по ...
 Review of Medical Microbiology and Immunology
Review of Medical Microbiology and Immunology To put your preparation for USMLE Step 1 and course exams on the fast track, only one resource will do: «Review of Medical Microbiology and ...