В то время как искусственная липидная мембрана для ионов практически не проницаема, биологические мембраны содержат «ионные каналы», по которым отдельные ионы избирательно проникают через мембрану (см. Транспортные процессы). Проницаемость и полярность мембраны зависят от электрохимического градиента, то есть от концентраций ионов по обе стороны мембраны (концентрационного градиента) и от разности электрических потенциалов между внутренней и внешней сторонами мембраны (мембранного потенциала).
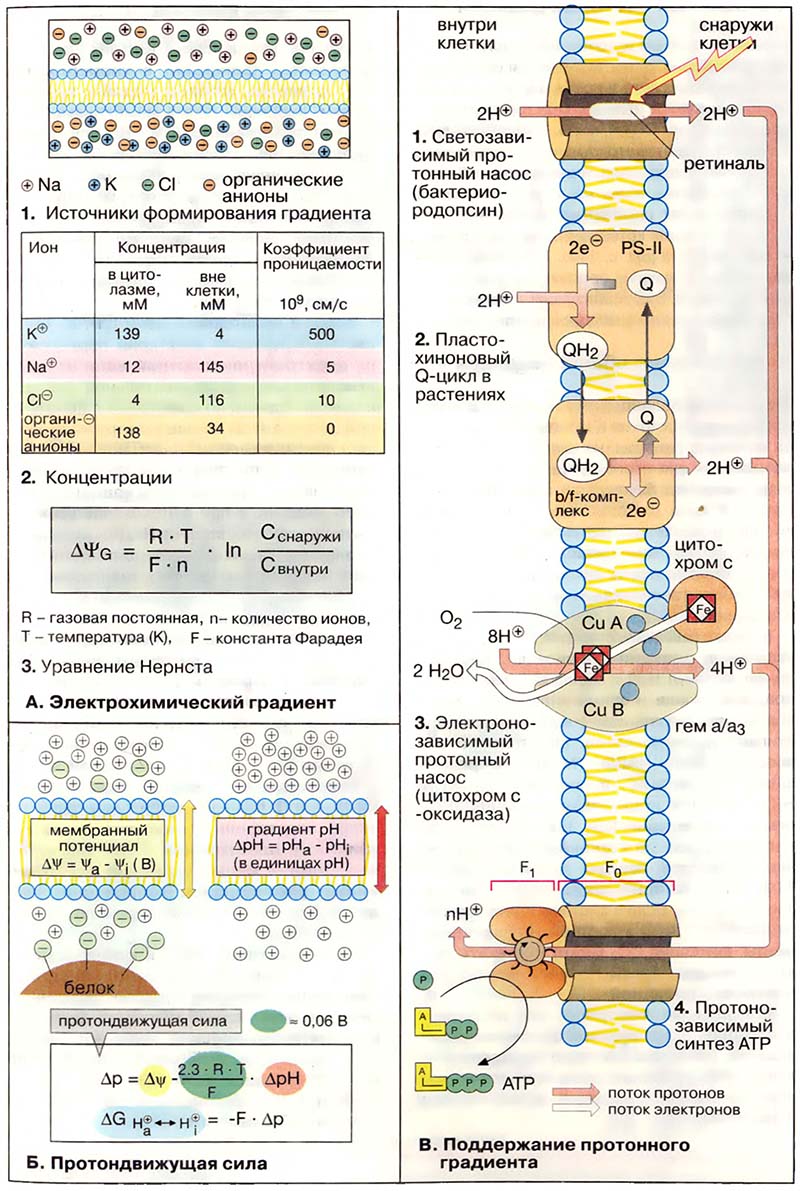
В состоянии покоя клеток мембранный потенциал (потенциал покоя, см. Потенциал покоя и потенциал действия) составляет от −0,05 до −0,09 В, то есть на внутренней стороне плазматической мембраны преобладает избыток отрицательных зарядов. Потенциал покоя обеспечивается прежде всего катионами Na+ и K+, а также органическими анионами и ионом Cl- (1). Концентрации снаружи и внутри клетки и коэффициенты проницаемости этих ионов приведены в таблице (2).
Распределение ионов между внешней средой и внутренним объёмом клетки описывается уравнением Нернста (3), где ΔΨG — трансмембранный потенциал (в вольтах, В), то есть разность электрических потенциалов между двумя сторонами мембраны при отсутствии транспорта ионов через мембрану (потенциал равновесия). Для одновалентных ионов при 25°С множитель RT/Fn равен 0,026 В. Вместе с тем из таблицы (2) следует, что для ионов K+ ΔΨG примерно равно −0,09 В, т. е. величина того же порядка, что и потенциал покоя. Для ионов Na+, напротив, ΔΨG ≈ +0,07 В, то есть выше, чем потенциал покоя. Поэтому ионы Na+ поступают в клетку при открытии Na+-канала. Неравенство концентраций ионов Na+ и K+ постоянно поддерживается Na+/K+-АТФ-азой при расходовании АТФ (см. Транспортные белки).
В состоянии покоя клеток мембранный потенциал (потенциал покоя, см. Потенциал покоя и потенциал действия) составляет от −0,05 до −0,09 В, то есть на внутренней стороне плазматической мембраны преобладает избыток отрицательных зарядов. Потенциал покоя обеспечивается прежде всего катионами Na+ и K+, а также органическими анионами и ионом Cl- (1). Концентрации снаружи и внутри клетки и коэффициенты проницаемости этих ионов приведены в таблице (2).
Распределение ионов между внешней средой и внутренним объёмом клетки описывается уравнением Нернста (3), где ΔΨG — трансмембранный потенциал (в вольтах, В), то есть разность электрических потенциалов между двумя сторонами мембраны при отсутствии транспорта ионов через мембрану (потенциал равновесия). Для одновалентных ионов при 25°С множитель RT/Fn равен 0,026 В. Вместе с тем из таблицы (2) следует, что для ионов K+ ΔΨG примерно равно −0,09 В, т. е. величина того же порядка, что и потенциал покоя. Для ионов Na+, напротив, ΔΨG ≈ +0,07 В, то есть выше, чем потенциал покоя. Поэтому ионы Na+ поступают в клетку при открытии Na+-канала. Неравенство концентраций ионов Na+ и K+ постоянно поддерживается Na+/K+-АТФ-азой при расходовании АТФ (см. Транспортные белки).
Статьи раздела «Сохранение энергии на мембранах»:
- Сохранение энергии на мембранах
- А. Электрохимический градиент
- Б. Протондвижущая сила
- В. Поддержание протонного градиента
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
Исследования, проводимые на микроорганизмах, внесли немалый вклад в изучение ...
В монографии рассматривается история развития учения об «антропотоксинах», ...
 Molecular Biology of the Cell: The Problems Book
Molecular Biology of the Cell: The Problems Book The Problems Book helps students appreciate the ways in which experiments and simple calculations can lead to an understanding of how cells work by ...
 Introductory Microbiology
Introductory Microbiology As a component of biology, Plant Pathology enjoyed a prestigious position and its applied aspects; plant disease management was an integral part of ...