В аминокислотах содержатся по крайней мере две ионогенные группы и, следовательно, их суммарный заряд зависит от pH среды. У карбоксильных групп при Cα pKa лежат в диапазоне 1,8-2,8, т.е.кислотные свойства у этих групп выражены сильнее, чем у незамещённых монокарбоновых кислот. pKa α-аминогрупп также различны и составляют 8,8-10,6. Кислые и основные аминокислоты несут в боковой цепи дополнительные ионогенные группы (pKa этих групп приведены на Аминокислоты: физические и химические свойства). Суммарный заряд пептидов и белков зависит главным образом от ионогенных групп боковых цепей, поскольку α-COOH- и α-NH2-группы принимают участие в образовании пептидных связей.
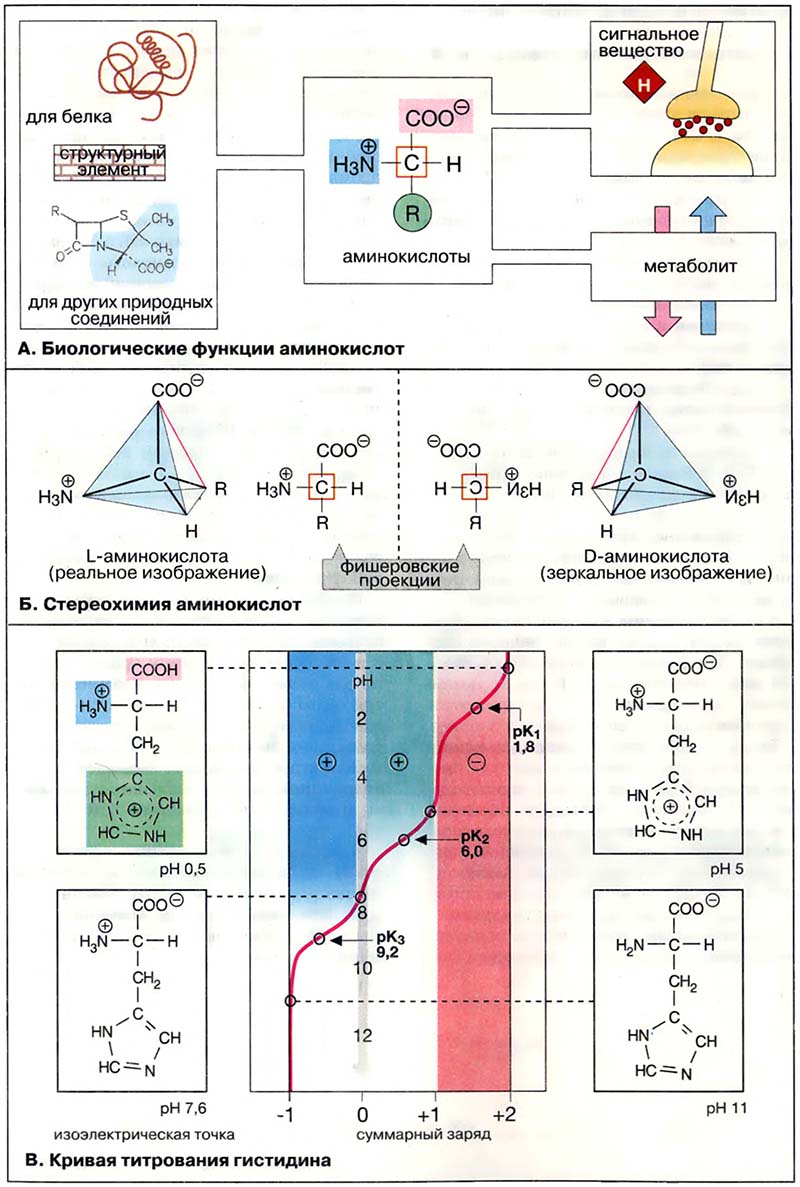
Зависимость заряда аминокислоты от pH среды хорошо видна на примере гистидина. В гистидине наряду с карбоксильной и аминогруппой при Cα pKa 1,8 и 9,2 соответственно) присутствует имидазольный остаток с pKa 6,0. Поэтому при повышении pH среды заряд гистидина изменяется от +2 до −1. При pH 7,6 суммарный заряд равен нулю, несмотря на то что в молекуле гистидина имеются две полностью ионизированные группы. Величина pH, при которой суммарный заряд равен нулю, называется изоэлектрической точкой.
В изоэлектрической точке гистидин является цвиттер-ионом, т. е. молекула обладает свойствами как аниона, так и катиона. В нейтральной области pH большинство аминокислот также являются цвиттер-ионами.
Зависимость заряда аминокислоты от pH среды хорошо видна на примере гистидина. В гистидине наряду с карбоксильной и аминогруппой при Cα pKa 1,8 и 9,2 соответственно) присутствует имидазольный остаток с pKa 6,0. Поэтому при повышении pH среды заряд гистидина изменяется от +2 до −1. При pH 7,6 суммарный заряд равен нулю, несмотря на то что в молекуле гистидина имеются две полностью ионизированные группы. Величина pH, при которой суммарный заряд равен нулю, называется изоэлектрической точкой.
В изоэлектрической точке гистидин является цвиттер-ионом, т. е. молекула обладает свойствами как аниона, так и катиона. В нейтральной области pH большинство аминокислот также являются цвиттер-ионами.
Статьи раздела «Аминокислоты: физические и химические свойства»:
- А. Биологические функции аминокислот
- Б. Стереохимия аминокислот
- В. Кривая титрования гистидина
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
Исследования, проводимые на микроорганизмах, внесли немалый вклад в изучение ...
Учебник состоит из четырёх частей, включающих 15 глав, в которых изложены вопросы ...
 Методы в молекулярной биофизике. Структура. Функция. Динамика. В 2 томах. Том 2
Методы в молекулярной биофизике. Структура. Функция. Динамика. В 2 томах. Том 2 Учебное пособие посвящено современному описанию физико-химических подходов, ...
 NMR Studies of Structural Motifs: Protein Folding and Ligand Binding
NMR Studies of Structural Motifs: Protein Folding and Ligand Binding NMR of Structural Motifs: The agrin G3 domain is critical in development and maintenance of the neuromuscular junction. G3 binds -dystroglycan and ...