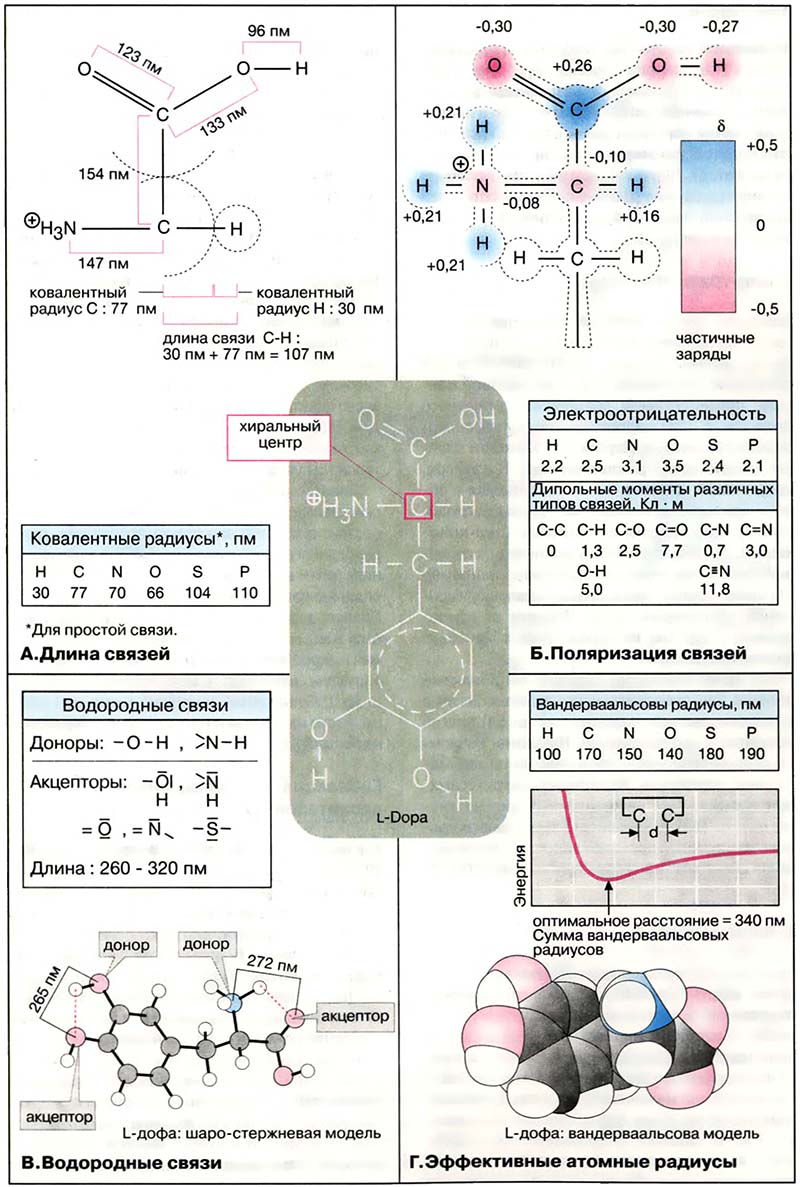
Для обозначения расстояний между атомами в молекуле используется понятие ковалентный радиус. Длина простой связи является величиной аддитивной: она примерно равна сумме ковалентных радиусов двух атомов. Двойная связь на 10-20 % короче простой связи. В последнее время атомные радиусы и расстояние между атомами принято выражать в пикометрах (пм, 1 пм = 10-12 м). Ранее длину связей представляли в ангстремах (Å , 1 Å = 100 пм).
Статьи раздела «Строение молекул»:
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Биохимия человека (комплект из 2 книг)
Биохимия человека (комплект из 2 книг) Настоящий учебник биологической и медицинской химии и молекулярной биологии ...
В стенограмме публичной лекции характеризуется метод тканевых культур и ...
Учебник состоит из четырёх частей, включающих 15 глав, в которых изложены вопросы ...
 Откровенная наука. Беседы с корифеями биохимии и медицинской химии
Откровенная наука. Беседы с корифеями биохимии и медицинской химии Книга И. Харгиттаи состоит из 36 бесед с выдающимися учёными XX века, работавшими в ...