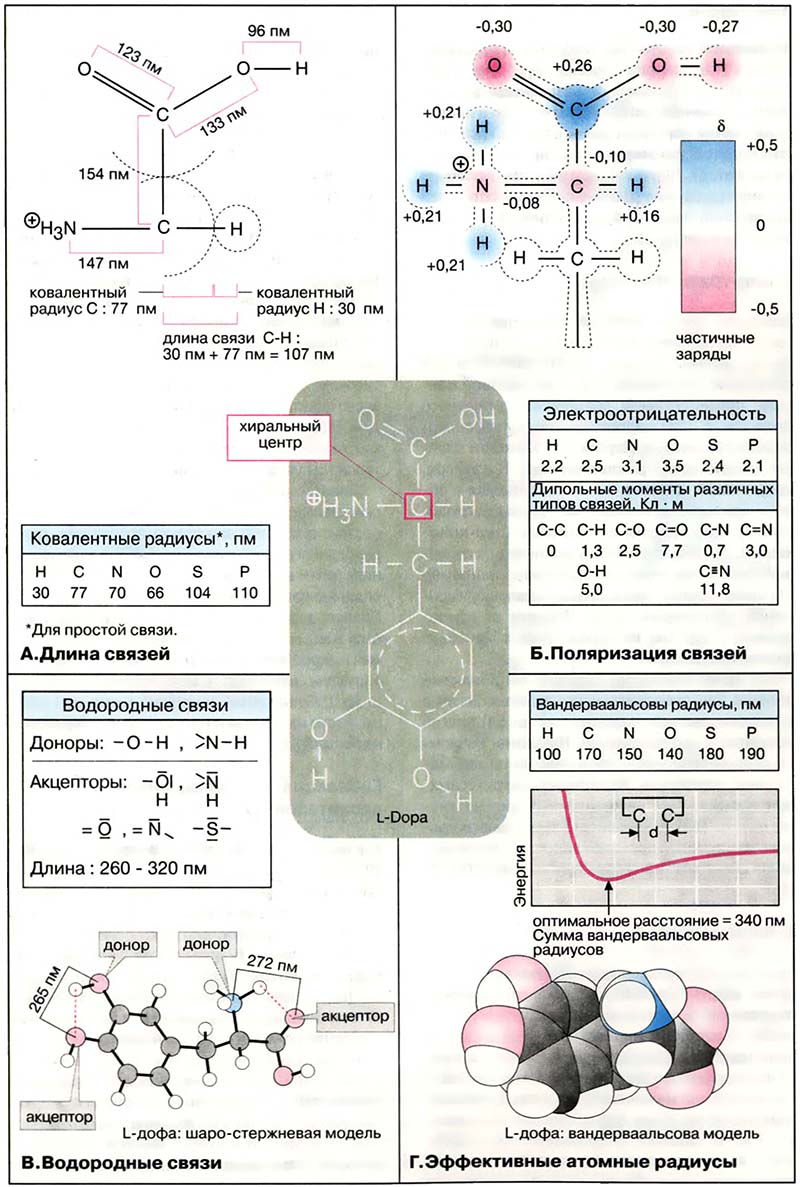
Особый тип нековалентной связи — водородная связь — имеет в биохимии исключительно важное значение. В образовании водородной связи принимают участие атомы водорода OH-, NH- и SH-групп (так называемых доноров водородной связи), которые взаимодействуют со свободной парой электронов атомов-акцепторов (например, O, N или S). Энергия водородной связи составляет 10-40 кДж/моль, что значительно меньше энергии ковалентной связи (меньше 400 кДж/моль). Однако многочисленные водородные связи вносят существенный вклад в стабилизацию структуры многих макромолекул (см. Глюконеогенез, Дезоксирибонуклеиновые кислоты). Например, L-дофа может образовывать две внутримолекулярные водородные связи. На шаро-стержневой модели L-дофа водородные мостики указаны штрихами.
Статьи раздела «Строение молекул»:
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
В монографии рассматривается история развития учения об «антропотоксинах», ...
 Методы в молекулярной биофизике. Структура. Функция. Динамика. В 2 томах. Том 2
Методы в молекулярной биофизике. Структура. Функция. Динамика. В 2 томах. Том 2 Учебное пособие посвящено современному описанию физико-химических подходов, ...
 Введение в биофизическую химию
Введение в биофизическую химию Книга представляет собой руководство по биофизической химии, в котором кратко и ...
Москва, 1955 год. Академия наук СССР. Издательский переплёт. Сохранность хорошая. На ...