Электроны, передаваемые НАДН (NADH), не переносятся прямо на кислород. Они проходят по меньшей мере десять промежуточных окислительно-восстановительных систем, большинство из которых это связанные простетические группы в комплексах I, III и IV. Прежде всего поражает большое число коферментов, принимающих участие в переносе электронов. Как показано в статье Фосфолипиды и гликолипиды, изменение свободной энергии ΔG в реакциях восстановления зависит только от разности окислительно-восстановительных потенциалов донора и акцептора. Наличие дополнительных окислительно-восстановительных систем между НАДН и O2 не приводит к изменению свободной энергии реакции. Общая величина энергии реакции (более 200 кДж/моль) разбивается на небольшие и более удобные «пакеты», величина которых определяется разностью окислительно-восстановительных потенциалов соответствующих промежуточных продуктов. Предполагается, что это разделение на пакеты обеспечивает дыхательной цепи удивительно высокий выход энергии, составляющий примерно 60 %.
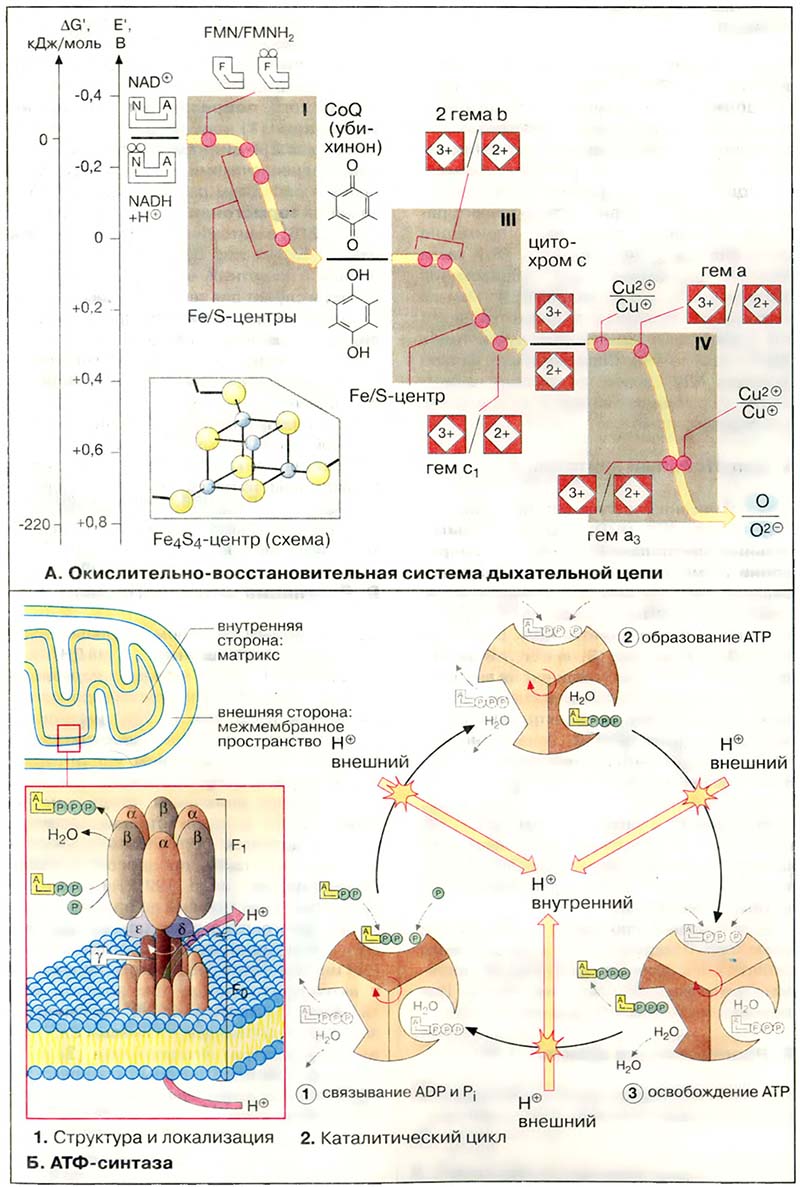
На схеме представлены основные окислительно-восстановительные системы митохондриального электронного транспорта и их приблизительные окислительно-восстановительные потенциалы. Эти потенциалы важны для переноса электронов, так как для обеспечения спонтанного переноса члены окислительно-восстановительного ряда должны располагаться в порядке возрастания потенциалов (см. Методы выделения и анализа белков).
В комплексе I электроны переносятся от НАДН на ФМН (FMN, см. Устройство и функционирование эндоплазматического ретикулума и аппарата Гольджи), а затем на железосодержащие белки (Fe/S-центры). Эти окислительно-восстановительные системы стабильны только в составе молекул белков. Они могут содержать от 2 до 6 ионов железа, образующих комплексы различного состава с неорганическим сульфидом и SH-группами остатков цистеина. На схеме показана структура так называемого Fe4S4-центра.
В переносе электронов принимают участие различные типы гемов. Гемы типа b соответствуют гемоглобинам (см. Транспорт газов). Гем с ковалентно связан с белком, в то время кактетрапиррольное кольцо гема a изопренилировано и несёт формильную группу. В комплексе IV непосредственно с кислородом взаимодействуют ион меди (CuB) и гем a3. Свойства кофермента Q и цитохрома с рассмотрены на Дыхательная цепь.
На схеме представлены основные окислительно-восстановительные системы митохондриального электронного транспорта и их приблизительные окислительно-восстановительные потенциалы. Эти потенциалы важны для переноса электронов, так как для обеспечения спонтанного переноса члены окислительно-восстановительного ряда должны располагаться в порядке возрастания потенциалов (см. Методы выделения и анализа белков).
В комплексе I электроны переносятся от НАДН на ФМН (FMN, см. Устройство и функционирование эндоплазматического ретикулума и аппарата Гольджи), а затем на железосодержащие белки (Fe/S-центры). Эти окислительно-восстановительные системы стабильны только в составе молекул белков. Они могут содержать от 2 до 6 ионов железа, образующих комплексы различного состава с неорганическим сульфидом и SH-группами остатков цистеина. На схеме показана структура так называемого Fe4S4-центра.
В переносе электронов принимают участие различные типы гемов. Гемы типа b соответствуют гемоглобинам (см. Транспорт газов). Гем с ковалентно связан с белком, в то время кактетрапиррольное кольцо гема a изопренилировано и несёт формильную группу. В комплексе IV непосредственно с кислородом взаимодействуют ион меди (CuB) и гем a3. Свойства кофермента Q и цитохрома с рассмотрены на Дыхательная цепь.
Статьи раздела «Синтез АТФ»:
- Синтез АТФ
- А. Окислительно-восстановительная система дыхательной цепи
- Б. АТФ-синтаза
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 NMR Studies of Structural Motifs: Protein Folding and Ligand Binding
NMR Studies of Structural Motifs: Protein Folding and Ligand Binding NMR of Structural Motifs: The agrin G3 domain is critical in development and maintenance of the neuromuscular junction. G3 binds -dystroglycan and ...
В книге обобщён большой опыт, накопленный за последние годы в области применения ...
В стенограмме публичной лекции характеризуется метод тканевых культур и ...
 Методы в молекулярной биофизике. Структура. Функция. Динамика. В 2 томах. Том 2
Методы в молекулярной биофизике. Структура. Функция. Динамика. В 2 томах. Том 2 Учебное пособие посвящено современному описанию физико-химических подходов, ...