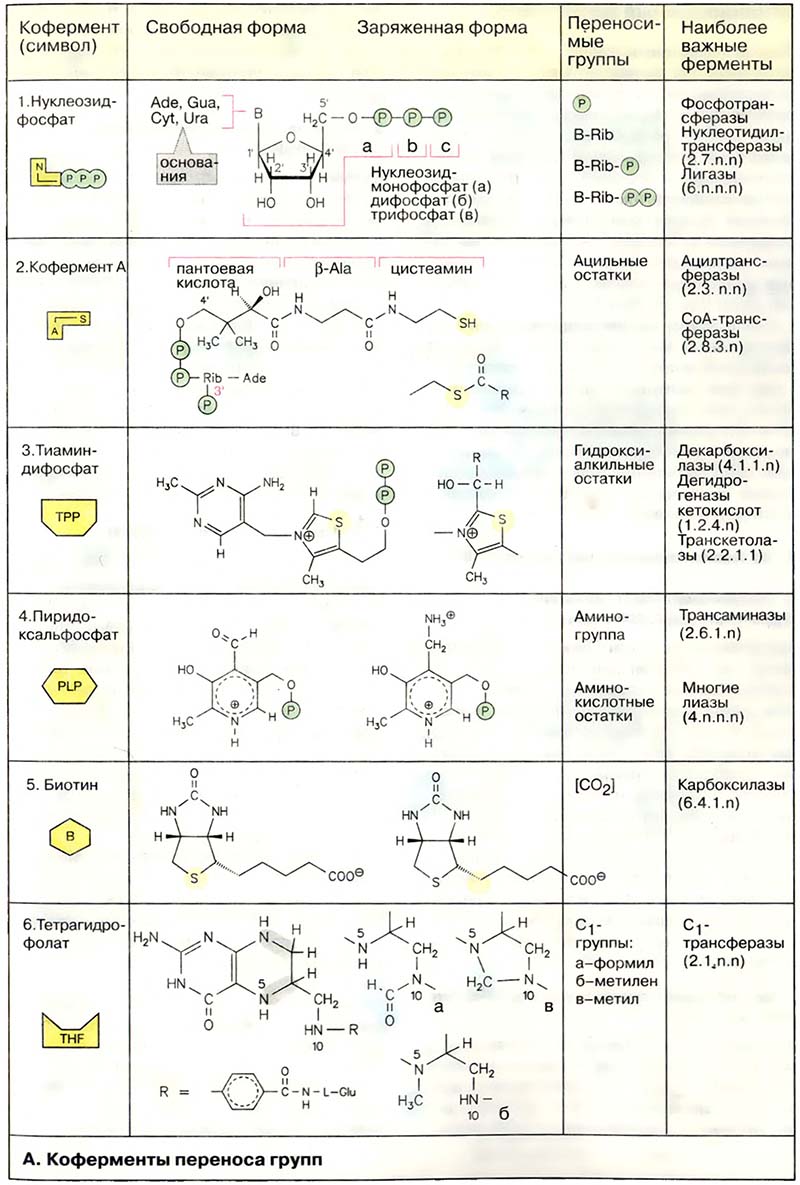
Нуклеозидфосфаты (1) являются не только исходными соединениями в биосинтезе нуклеиновых кислот, они обладают также функциями коферментов, служат для запасания энергии и участвуют в цепи переноса энергии (см. Деградация порфиринов) в эндоэргических процессах. Метаболические интермедиаты часто становятся реакционноспособными («активированными») при присоединении фосфатсодержащих остатков (фосфорилирование). Так, присоединение нуклеозиддифосфатных остатков делает реакционноспособными исходные соединения в синтезе полисахаридов и липидов (см. Сортировка белков). Лигазы катализируют сшивание соединений за счёт энергии нуклеозидтрифосфатов.
Остатки жирных кислот активируются путём переноса на кофермент A (2). В коферменте A пантетеин через фосфоангидридную связь присоединён к 3′-фосфо-АДФ. Пантетеин состоит из трёх компонентов, связанных амидными связями: пантоевой кислоты, β-аланина и цистеамина, то есть двух биогенных аминов, образованных путём де-карбоксилирования соответственно аспартата и цистеина (см. Механизм действия гидрофильных гормонов). Пантотеновая кислота, образованная из пантоевой кислоты и β-аланина, в организме человека играет роль витамина (см. Водорастворимые витамины. I). При реакции тиоловой группы остатка цистеамина с карбоновой кислотой образуется тиол-сложно-эфирная связь, как, например, в ацетил-КоА (ацетил-СоА). Эта реакция высоко эндоэргична и поэтому сопряжена с экзоэргическими процессами. Тиоэфир, каким является ацил-КоА, представляет собой активированную форму карбоновой кислоты, так как образующий её ацильный остаток может легко переноситься на другую молекулу. Этот принцип часто используется при метаболических превращениях.
Тиаминдифосфат (ТРР, 3) активирует альдегиды и кетоны и переносит их в виде гидроксиалкильных групп на другую молекулу. Этот способ переноса важен, например, в транскетолазной реакции (см. Моча). Гидроксиалкильные остатки участвуют также в декарбоксилировании кетокислот. Они либо высвобождаются в виде альдегидов, либо переносятся на липоамидные остатки, как в случае дегидрогеназ 2-кетокислот (см. Процессы пищеварения).
Пиридоксальфосфат (PLP) (4) — наиболее важный кофермент в метаболизме аминокислот. Его роль при трансаминировании будет подробно рассмотрена в статье Гидрофильные гормоны. Пиридоксальфосфат принимает участие и в других реакциях аминокислот, таких, как декарбоксилирование и дегидратирование. Представленная здесь альдегидная форма в свободном виде не встречается. В отсутствие субстрата альдегидная группа связана с аминогруппой лизинового остатка фермента в виде альдимина («шиффово основание»).
Карбоксилазы содержат в качестве кофермента биотин (5). Он связан амидной связью с боковой цепью лизинового остатка фермента. Биотин реагирует с гидрокарбонатом (HCO3-) в присутствии АТФ с образованием N-карбоксибиотина. Эта активированная форма диоксида углерода может быть перенесена на другую молекулу. Примерами биотинзависимых реакций являются образование оксалоацетата из пирувата (см. Реабсорбция электролитов и воды) и синтез малонил-КоА из ацетил-КоА (см. Питание. Органические вещества).
Тетрагидрофолат [ТГФ (THF), 6] является коферментом, который может переносить C1-остатки в различных состояниях окисления. ТГФ образуется из витамина фолиевой кислоты двойным гидрированием птеринового кольца. C1-фрагменты присоединяются к N-5, N-10 или к обоим атомам азота. Наиболее важными производными тетрагидрофолата являются:
а) N10-формил-ТГФ, в котором C1-остаток находится в виде карбоксильной группы,
б) N5, N10-метилен-ТГФ, в котором C1-остаток находится в виде альдегида
и в) N5-Meтил-THF, где C1 находится в виде спирта. Переносимый ТГФ C1-фрагмент играет важную роль, например, в синтезе пуриновых нуклеотидов (см. Цитостатики), дезокситимидинмонофосфата (см. Биосинтез нуклеотидов) и метионина.
Остатки жирных кислот активируются путём переноса на кофермент A (2). В коферменте A пантетеин через фосфоангидридную связь присоединён к 3′-фосфо-АДФ. Пантетеин состоит из трёх компонентов, связанных амидными связями: пантоевой кислоты, β-аланина и цистеамина, то есть двух биогенных аминов, образованных путём де-карбоксилирования соответственно аспартата и цистеина (см. Механизм действия гидрофильных гормонов). Пантотеновая кислота, образованная из пантоевой кислоты и β-аланина, в организме человека играет роль витамина (см. Водорастворимые витамины. I). При реакции тиоловой группы остатка цистеамина с карбоновой кислотой образуется тиол-сложно-эфирная связь, как, например, в ацетил-КоА (ацетил-СоА). Эта реакция высоко эндоэргична и поэтому сопряжена с экзоэргическими процессами. Тиоэфир, каким является ацил-КоА, представляет собой активированную форму карбоновой кислоты, так как образующий её ацильный остаток может легко переноситься на другую молекулу. Этот принцип часто используется при метаболических превращениях.
Тиаминдифосфат (ТРР, 3) активирует альдегиды и кетоны и переносит их в виде гидроксиалкильных групп на другую молекулу. Этот способ переноса важен, например, в транскетолазной реакции (см. Моча). Гидроксиалкильные остатки участвуют также в декарбоксилировании кетокислот. Они либо высвобождаются в виде альдегидов, либо переносятся на липоамидные остатки, как в случае дегидрогеназ 2-кетокислот (см. Процессы пищеварения).
Пиридоксальфосфат (PLP) (4) — наиболее важный кофермент в метаболизме аминокислот. Его роль при трансаминировании будет подробно рассмотрена в статье Гидрофильные гормоны. Пиридоксальфосфат принимает участие и в других реакциях аминокислот, таких, как декарбоксилирование и дегидратирование. Представленная здесь альдегидная форма в свободном виде не встречается. В отсутствие субстрата альдегидная группа связана с аминогруппой лизинового остатка фермента в виде альдимина («шиффово основание»).
Карбоксилазы содержат в качестве кофермента биотин (5). Он связан амидной связью с боковой цепью лизинового остатка фермента. Биотин реагирует с гидрокарбонатом (HCO3-) в присутствии АТФ с образованием N-карбоксибиотина. Эта активированная форма диоксида углерода может быть перенесена на другую молекулу. Примерами биотинзависимых реакций являются образование оксалоацетата из пирувата (см. Реабсорбция электролитов и воды) и синтез малонил-КоА из ацетил-КоА (см. Питание. Органические вещества).
Тетрагидрофолат [ТГФ (THF), 6] является коферментом, который может переносить C1-остатки в различных состояниях окисления. ТГФ образуется из витамина фолиевой кислоты двойным гидрированием птеринового кольца. C1-фрагменты присоединяются к N-5, N-10 или к обоим атомам азота. Наиболее важными производными тетрагидрофолата являются:
а) N10-формил-ТГФ, в котором C1-остаток находится в виде карбоксильной группы,
б) N5, N10-метилен-ТГФ, в котором C1-остаток находится в виде альдегида
и в) N5-Meтил-THF, где C1 находится в виде спирта. Переносимый ТГФ C1-фрагмент играет важную роль, например, в синтезе пуриновых нуклеотидов (см. Цитостатики), дезокситимидинмонофосфата (см. Биосинтез нуклеотидов) и метионина.
Статьи раздела «Коферменты переноса групп»:
- Коферменты переноса групп
- А. Коферменты переноса групп
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
В книге даётся богатейший, хорошо систематизированный справочный материал по ...
 Фотосинтез. В 2 томах (комплект)
Фотосинтез. В 2 томах (комплект) Книга, написанная в основном американскими авторами, представляет собой ...
 Влияние тяжелых металлов на процессы биохимического окисления органических веществ
Влияние тяжелых металлов на процессы биохимического окисления органических веществ В научной монографии рассмотрены основные направления очистки сточных вод, ...
