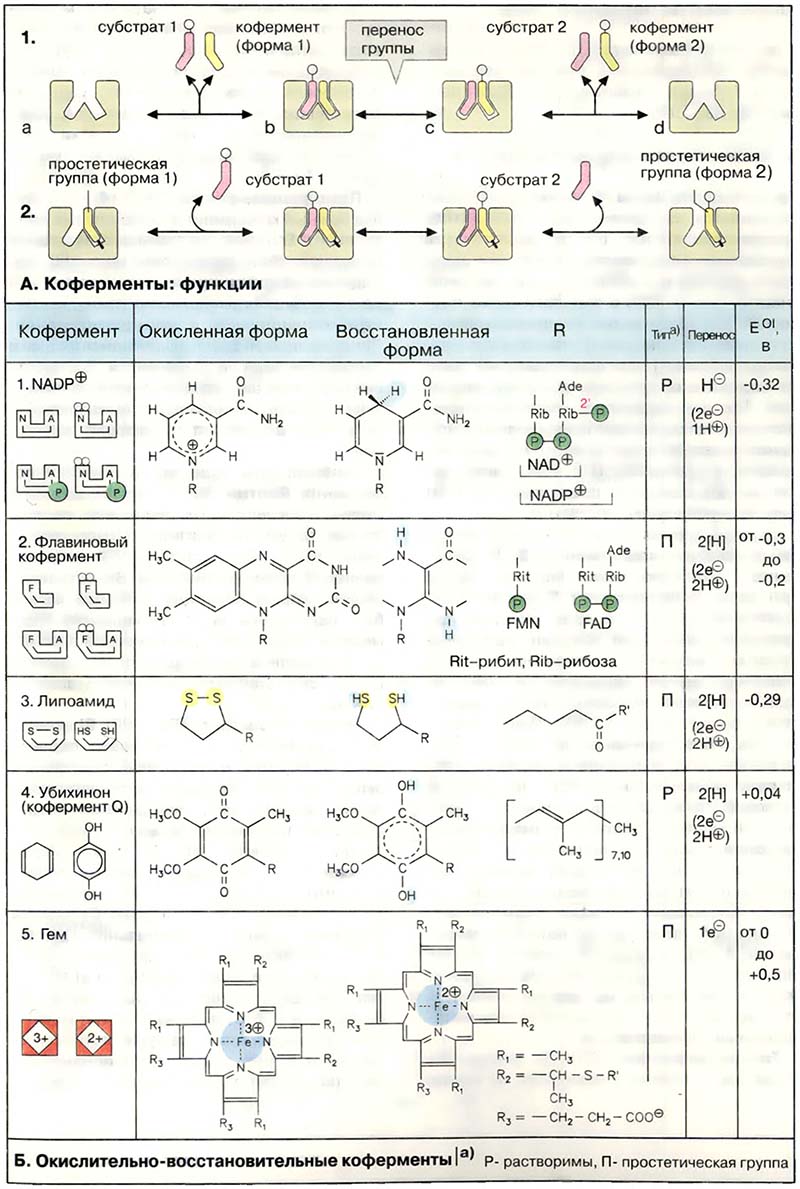
Все оксидоредуктазы (см. Деградация порфиринов) нуждаются в коферменте. Наиболее важные коферменты представлены на схеме. Они могут действовать в растворимой форме (Р) или в виде простетической группы (П). Окислительновосстановительные реакции, наряду с переносом электронов, часто включают перенос одного или двух протонов. Поэтому обычно принято говорить о переносе восстановительных эквивалентов. Стандартный потенциал Е°’ простетической группы (см. Фосфолипиды и гликолипиды) может значительно отличаться в зависимости от окружения в молекуле фермента.
Пиридиннуклеотиды НАД+ (NAD+) и НАДФ+ (NADP+) (1) широко распространены как коферменты дегидрогеназ. Они переносят гидрид-ион (2e- и 1 Н+, см. Митохондрии: структура и функции) и действуют всегда в растворимой форме. НАД+ передаёт восстановительный эквивалент из катаболического пути в дыхательную цепь и тем самым участвует в энергетическом обмене. МАДФ+, напротив, является самым важным восстановителем при биосинтезе (см. Геном).
Флавиновые коферменты ФМН (FMN) и ФАД (FAD) (2, см. Трансаминирование и дезаминирование) найдены в дегидрогеназах, оксидазах и монооксигеназах. Обычно оба соединения ковалентно связаны с ферментами. Активной группой обоих ко-ферментов является флавин (изоаллоксазин), имеющий сопряжённую систему из трёх колец, которая может при восстановлении принимать два электрона и два протона. В ФМН к флавину присоединён фосфорилированный полиол рибит. ФАД состоит из ФМН, связанного с АМФ. Оба соединения являются функционально близкими коферментами.
В липоевой кислоте (3) функцию окислительно-восстановительного центра выполняет внутримолекулярный дисульфидный мостик. Активная липоевая кислота ковалентно связана с остатком лизина (R′) молекулы фермента. Липоевая кислота прежде всего участвует в окислительном декарбоксилировании 2-кетокислот (см. Кислотно-основной баланс). Дисульфидный мостик также содержится в пептидном коферменте глутатионе (см. Эритроциты: обмен веществ).
Функция убихинона (кофермента Q, 4) как переносчика восстановительного эквивалента в дыхательной цепи будет рассмотрена в статье Белки главного комплекса гисто-совместимости. При восстановлении хинон превращается в ароматический гидрохинон (убихинол). Похожие системы хинон/гидрохинон принимают участие в реакциях фотосинтеза (см. Липопротеины). К этому классу окислительно-восстановительных систем принадлежат также витамины Е и K (см. Жирорастворимые витамины).
Группа гема (5) является окислительно-восстановительным кофактором в дыхательной цепи (см. Моноклональные антитела, иммуноанализ), фотосинтезе (см. Кровь: состав и функции), а также в монооксигеназах (см. Система цитохрома Р450) и пероксидазах. В отличие от гемоглобина в этих случаях ион железа меняет валентность. На рисунке показан гем в цитохроме с, ковалентно связанный с двумя остатками цистеина(R2)белка.
Пиридиннуклеотиды НАД+ (NAD+) и НАДФ+ (NADP+) (1) широко распространены как коферменты дегидрогеназ. Они переносят гидрид-ион (2e- и 1 Н+, см. Митохондрии: структура и функции) и действуют всегда в растворимой форме. НАД+ передаёт восстановительный эквивалент из катаболического пути в дыхательную цепь и тем самым участвует в энергетическом обмене. МАДФ+, напротив, является самым важным восстановителем при биосинтезе (см. Геном).
Флавиновые коферменты ФМН (FMN) и ФАД (FAD) (2, см. Трансаминирование и дезаминирование) найдены в дегидрогеназах, оксидазах и монооксигеназах. Обычно оба соединения ковалентно связаны с ферментами. Активной группой обоих ко-ферментов является флавин (изоаллоксазин), имеющий сопряжённую систему из трёх колец, которая может при восстановлении принимать два электрона и два протона. В ФМН к флавину присоединён фосфорилированный полиол рибит. ФАД состоит из ФМН, связанного с АМФ. Оба соединения являются функционально близкими коферментами.
В липоевой кислоте (3) функцию окислительно-восстановительного центра выполняет внутримолекулярный дисульфидный мостик. Активная липоевая кислота ковалентно связана с остатком лизина (R′) молекулы фермента. Липоевая кислота прежде всего участвует в окислительном декарбоксилировании 2-кетокислот (см. Кислотно-основной баланс). Дисульфидный мостик также содержится в пептидном коферменте глутатионе (см. Эритроциты: обмен веществ).
Функция убихинона (кофермента Q, 4) как переносчика восстановительного эквивалента в дыхательной цепи будет рассмотрена в статье Белки главного комплекса гисто-совместимости. При восстановлении хинон превращается в ароматический гидрохинон (убихинол). Похожие системы хинон/гидрохинон принимают участие в реакциях фотосинтеза (см. Липопротеины). К этому классу окислительно-восстановительных систем принадлежат также витамины Е и K (см. Жирорастворимые витамины).
Группа гема (5) является окислительно-восстановительным кофактором в дыхательной цепи (см. Моноклональные антитела, иммуноанализ), фотосинтезе (см. Кровь: состав и функции), а также в монооксигеназах (см. Система цитохрома Р450) и пероксидазах. В отличие от гемоглобина в этих случаях ион железа меняет валентность. На рисунке показан гем в цитохроме с, ковалентно связанный с двумя остатками цистеина(R2)белка.
Статьи раздела «Окислительно-восстановительные коферменты»:
- А. Коферменты: функции
- Б. Окислительно-восстановительные коферменты
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Histone H1 glycation and rutin metabolites as glycation inhibitors: Nuclear protein glycation in vivo and novel natural product AGE inhibitors
Histone H1 glycation and rutin metabolites as glycation inhibitors: Nuclear protein glycation in vivo and novel natural product AGE inhibitors Protein glycation, induced by hyperglycemia, is implicated in the appearance of diabetic complications and the aging process. Glycation involves the ...
 Biotechnology Annual R Volume 14 (Biotechnology Annual Review) (Biotechnology Annual Review)
Biotechnology Annual R Volume 14 (Biotechnology Annual Review) (Biotechnology Annual Review) Biotechnology is a diverse, complex, and rapidly evolving field. Students and experienced researchers alike face the challenges of staying on top of ...
 Microbiology with Diseases by Taxonomy with MasteringMicrobiology (3rd Edition)
Microbiology with Diseases by Taxonomy with MasteringMicrobiology (3rd Edition) The Third Edition of Microbiology with Diseases by Taxonomy is the most cutting-edge microbiology book available, offering unparalleled currency, ...
 Планета вирусов
Планета вирусов Вирусы — невидимые, но активные участники борьбы за место в биосфере Земли. С их ...