Определённые сочетания двугранных углов φ и ψ (см. Гликолиз) встречаются в белках довольно часто. Если множество последовательно связанных аминокислотных остатков принимает стандартные конформации, формируются вторичные структуры, стабилизированные водородными мостиками в пределах одной пептидной цепи или между соседними цепями. Если такая регулярная структура распространяется на достаточно большой фрагмент молекулы белка, такой белок образует механически прочные нити или волокна. Подобного рода структурные белки (см. Структурные белки) имеют характерный аминокислотный состав.
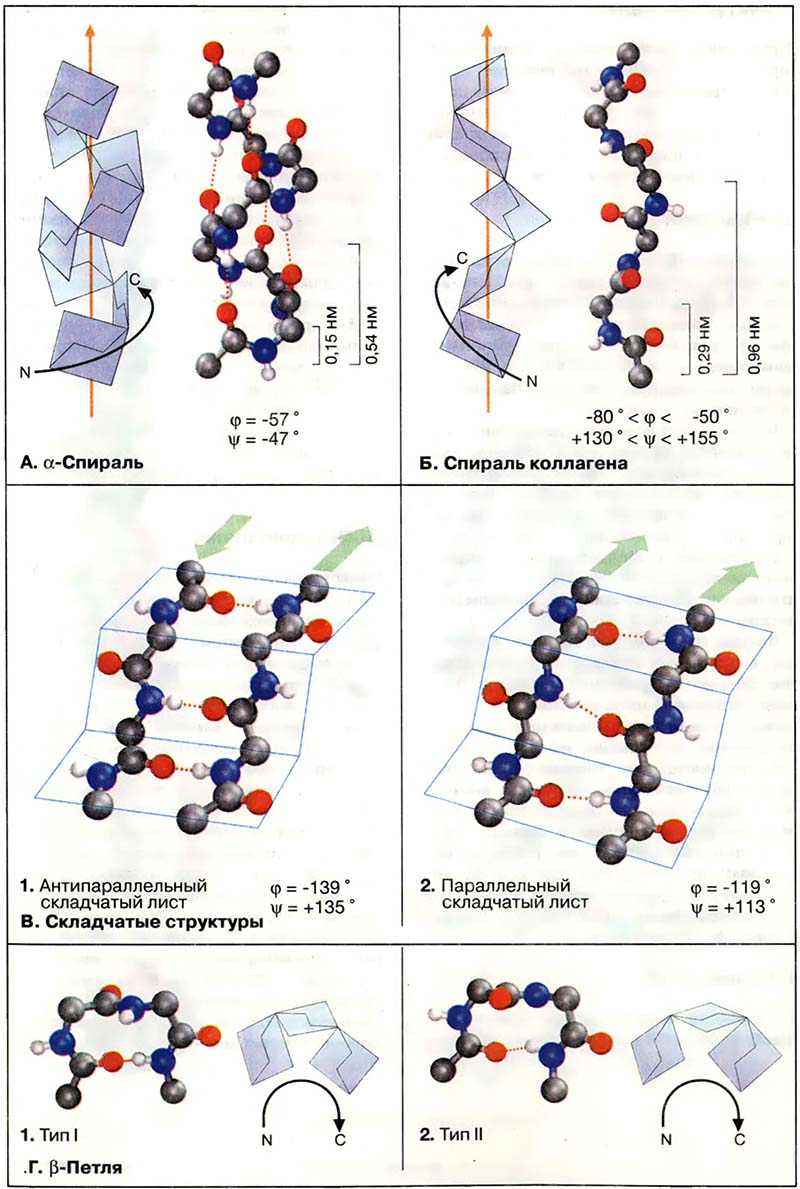
Здесь приведены основные элементы вторичных структур. На рисунках представлен остов полипептидной цепи, лишённый боковых цепей аминокислотных остатков. Для наглядности плоскости пептидных связей изображены в виде голубых пластин. Двугранные углы указанных структур приведены на конформационной карте Г1.
Здесь приведены основные элементы вторичных структур. На рисунках представлен остов полипептидной цепи, лишённый боковых цепей аминокислотных остатков. Для наглядности плоскости пептидных связей изображены в виде голубых пластин. Двугранные углы указанных структур приведены на конформационной карте Г1.
Статьи раздела «Вторичные структуры белков»:
- Вторичные структуры белков
- А. α-Спираль
- Б. Спираль коллагена
- В. Складчатые структуры
- Г. β-Петля
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Лекции по природоведческой микробиологии
Лекции по природоведческой микробиологии Книга основана на курсе лекций, прочитанных в МГУ им. М. В. Ломоносова в 1995-2002 гг. ...
 Review of Medical Microbiology and Immunology
Review of Medical Microbiology and Immunology To put your preparation for USMLE Step 1 and course exams on the fast track, only one resource will do: «Review of Medical Microbiology and ...
 Введение в молекулярную биологию
Введение в молекулярную биологию Задача предлагаемой книги состоит в ознакомлении читателей с важнейшими фактами ...
 Cell Biology: With STUDENT CONSULT Online Access
Cell Biology: With STUDENT CONSULT Online Access A masterful, richly illustrated introduction to the cell biology that you need to know.