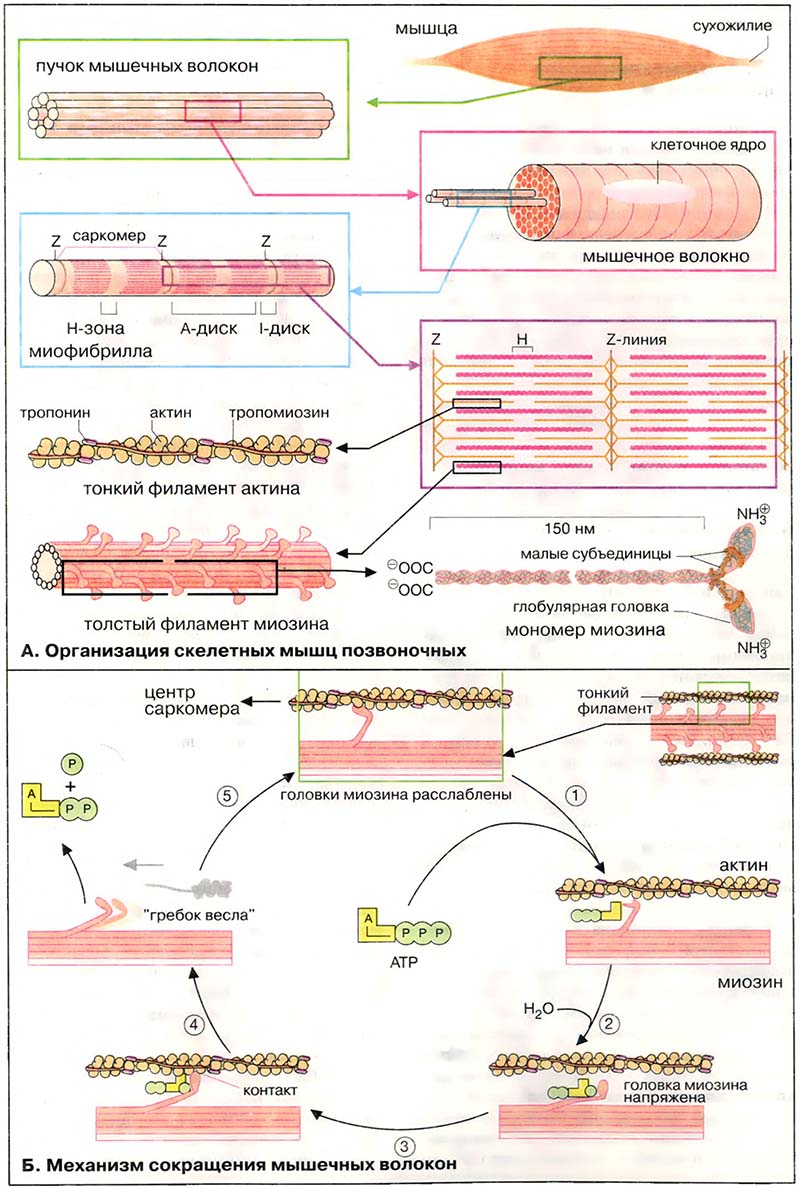
Скелетные поперечнополосатые мышцы позвоночных состоят из параллельных пучков мышечных волокон. Каждое волокно представляет собой одну большую многоядерную клетку. Большую часть объёма мышечных клеток занимают миофибриллы толщиной 1-2 мкм, простирающиеся на всю длину мышечного волокна. Поперечная исчерченность, характерная для миофибрилл скелетных мышц, связана с чередованием различных по толщине молекул.
Сократительные элементы, саркомеры, состоят из двух типов параллельных нитей, толстых филаментов миозина и тонких филаментов F-актина (см. Клеточные компоненты и цитоплазма). Крайние, более тёмные области A-дисков содержат как тонкие, так и толстые нити, тогда как центральная часть, Н-зона, содержит только нити миозина. Z-Линии (или Z-пластинки) соответствуют тем участкам, где тонкие нити крепятся к так называемым Z-дискам. Саркомером называется продольная единица, ограниченная двумя Z-линиями.
В количественном отношении наиболее важным белком миофибрилл является миозин (~65 % мышечного белка). Молекула миозина построена из шести субъединиц, двух идентичных тяжёлых цепей (2 × 223 кДа) и четырёх лёгких цепей (-20 кДа), связанных нековалентно. Каждая тяжёлая цепь миозина имеет форму длинного стержня длиной 150 нм с глобулярной головкой на N-конце и напоминает клюшку для гольфа (на схеме внизу справа). α-Спиральные участки двух тяжёлых цепей свёрнуты в двойную суперспираль, а четыре небольших субъединицы связаны с глобулярными головками. В мышечном волокне миозин образует толстые миозиновые филаменты, которые представляют собой пучки из сотен молекул миозина, расположенных параллельно. Головка молекулы миозина обладает Ca2+-зависимой АТФ-азной активностью (КФ 3.6.1.32), которая регулируется малыми субъединицами.
Главным белком тонких нитей является актин (42 кДа, −20-25 % мышечного белка). Фибриллярный F-актин является важным структурным элементом цитоскелета; он находится в равновесии с глобулярным G-актином.
Кроме этих двух белков система включает тропомиозин и комплекс тропонина. Нитевидный тропомиозин (64 кДа) связан с F-актином, охватывая примерно семь актиновых субъединиц. Тропонин (78 кДа) — комплекс, состоящий из трёх различных субъединиц (Т, C, I), способен связываться как с актином, так и с тропомиозином. Остальные белки, присутствующие в гораздо меньшем количестве, включают α- и β-актинин, десмин, коннектин (титин) и виментин.
Сократительные элементы, саркомеры, состоят из двух типов параллельных нитей, толстых филаментов миозина и тонких филаментов F-актина (см. Клеточные компоненты и цитоплазма). Крайние, более тёмные области A-дисков содержат как тонкие, так и толстые нити, тогда как центральная часть, Н-зона, содержит только нити миозина. Z-Линии (или Z-пластинки) соответствуют тем участкам, где тонкие нити крепятся к так называемым Z-дискам. Саркомером называется продольная единица, ограниченная двумя Z-линиями.
В количественном отношении наиболее важным белком миофибрилл является миозин (~65 % мышечного белка). Молекула миозина построена из шести субъединиц, двух идентичных тяжёлых цепей (2 × 223 кДа) и четырёх лёгких цепей (-20 кДа), связанных нековалентно. Каждая тяжёлая цепь миозина имеет форму длинного стержня длиной 150 нм с глобулярной головкой на N-конце и напоминает клюшку для гольфа (на схеме внизу справа). α-Спиральные участки двух тяжёлых цепей свёрнуты в двойную суперспираль, а четыре небольших субъединицы связаны с глобулярными головками. В мышечном волокне миозин образует толстые миозиновые филаменты, которые представляют собой пучки из сотен молекул миозина, расположенных параллельно. Головка молекулы миозина обладает Ca2+-зависимой АТФ-азной активностью (КФ 3.6.1.32), которая регулируется малыми субъединицами.
Главным белком тонких нитей является актин (42 кДа, −20-25 % мышечного белка). Фибриллярный F-актин является важным структурным элементом цитоскелета; он находится в равновесии с глобулярным G-актином.
Кроме этих двух белков система включает тропомиозин и комплекс тропонина. Нитевидный тропомиозин (64 кДа) связан с F-актином, охватывая примерно семь актиновых субъединиц. Тропонин (78 кДа) — комплекс, состоящий из трёх различных субъединиц (Т, C, I), способен связываться как с актином, так и с тропомиозином. Остальные белки, присутствующие в гораздо меньшем количестве, включают α- и β-актинин, десмин, коннектин (титин) и виментин.
Статьи раздела «Сократительная система»:
- А. Организация скелетных мышц позвоночных
- Б. Механизм сокращения мышечных волокон
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Books a la Carte Plus for Microbiology with Diseases by Taxonomy (3rd Edition)
Books a la Carte Plus for Microbiology with Diseases by Taxonomy (3rd Edition) The Third Edition of Microbiology with Diseases by Taxonomy is the most cutting-edge microbiology book available, offering unparalleled currency, ...
В книге собраны лучшие из современных методов выделения и анализа важнейшего ...
Учебное пособие, в котором авторы из США и Великобритании в доступной форме ...
 Молекулярное моделирование. Теория и практика
Молекулярное моделирование. Теория и практика В научном издании, написанном учёными из Германии, Франции и Швейцарии, имеющими ...