Наиболее важной буферной системой плазмы является бикарбонатный буфер, состоящий из слабой угольной кислоты (pK1 6,1) и её кислого аниона бикарбоната. Угольная кислота H2CO3 находится в равновесии со своим ангидридом CO2. Установление равновесия между обеими формами ускоряется ферментом карбонатдегидратазой («карбоангидразой»). При pH плазмы концентрации HCO3- и CO2 находятся в соотношении 20/1. Растворенный в крови CO2 равновесно обменивается с CO2 газовой фазы альвеол лёгких. Поэтому HCO3-/CO2--система является эффективной открытой буферной системой. Ускоренное или замедленное дыхание изменяет концентрацию CO2, что приводит к изменению pH плазмы (дыхательный ацидоз или соответственно алкалоз). Таким образом, лёгкие могут быстро и действенно влиять на pH плазмы без участия систем удаления протонов.
Белки плазмы и особенно гемоглобин эритроцитов (см. Транспорт газов) также способны присоединять протоны, поддерживая постоянство pH. Определённый вклад в буферные свойства крови вносит фосфат.
Белки плазмы и особенно гемоглобин эритроцитов (см. Транспорт газов) также способны присоединять протоны, поддерживая постоянство pH. Определённый вклад в буферные свойства крови вносит фосфат.
Статьи раздела «Кислотно-основной баланс»:
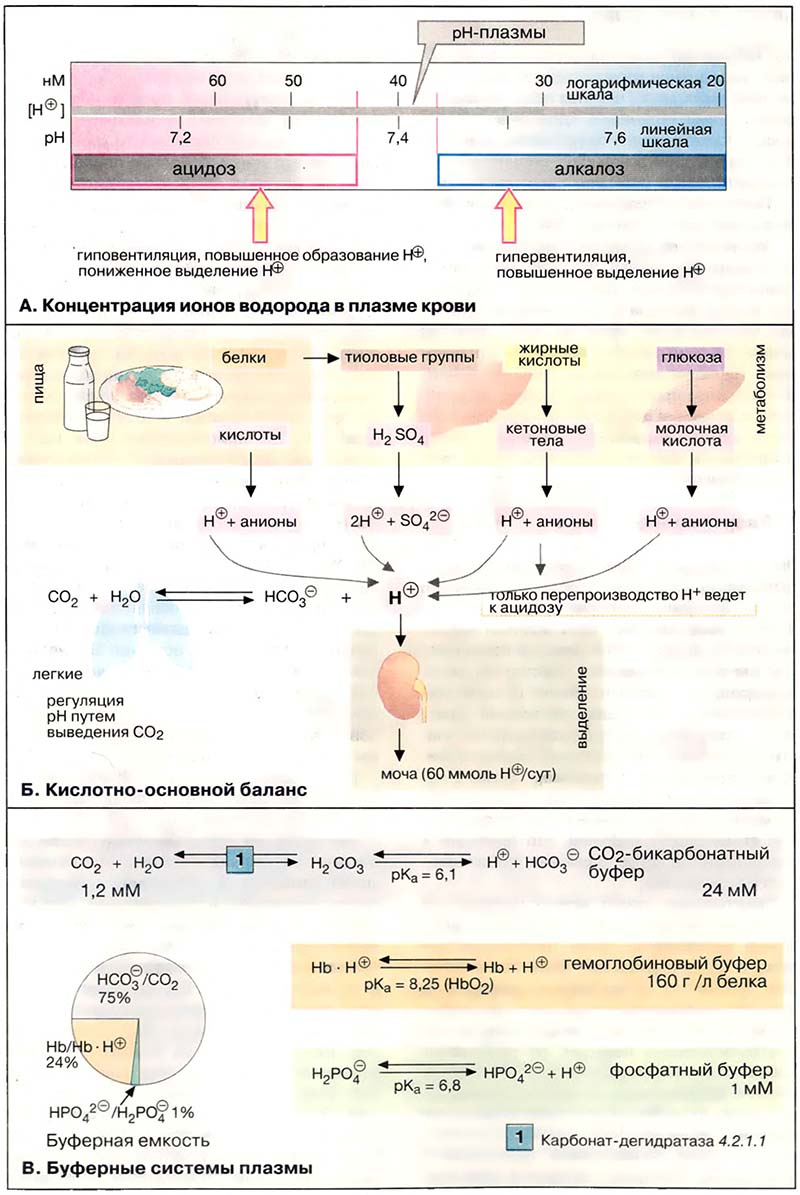
- А. Концентрация ионов водорода в плазме крови
- Б. Кислотно-основной баланс
- В. Буферные системы плазмы
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Анализ биологических последовательностей
Анализ биологических последовательностей Предлагаемая книга отражает современное состояние сравнительно новой, но весьма ...
 Микрокосм. E. coli и новая наука о жизни
Микрокосм. E. coli и новая наука о жизни Цитата «В начале XX в. учёные, стремясь познать природу жизни, начали исследовать ...
Монография посвящена одному из самых информативных методов физико-химической ...
