Синтаза жирных кислот позвоночных состоит из двух идентичных пептидных цепей, то есть представляет собой гомодимер. Каждая из двух пептидных цепей, представленных на рисунке в виде половинок шара, может катализировать семь различных реакций ([1] — [7]), из которых складывается синтез пальмитата. Пространственное объединение нескольких последовательных реакций в таком мультиферментном комплексе имеет ряд принципиальных преимуществ по сравнению с отдельными ферментами: предотвращаются конкурентные реакции, последовательные реакции согласованы как на конвейере, реакции протекают особенно эффективно благодаря высокой концентрации субстрата из-за незначительных потерь за счёт диффузии.
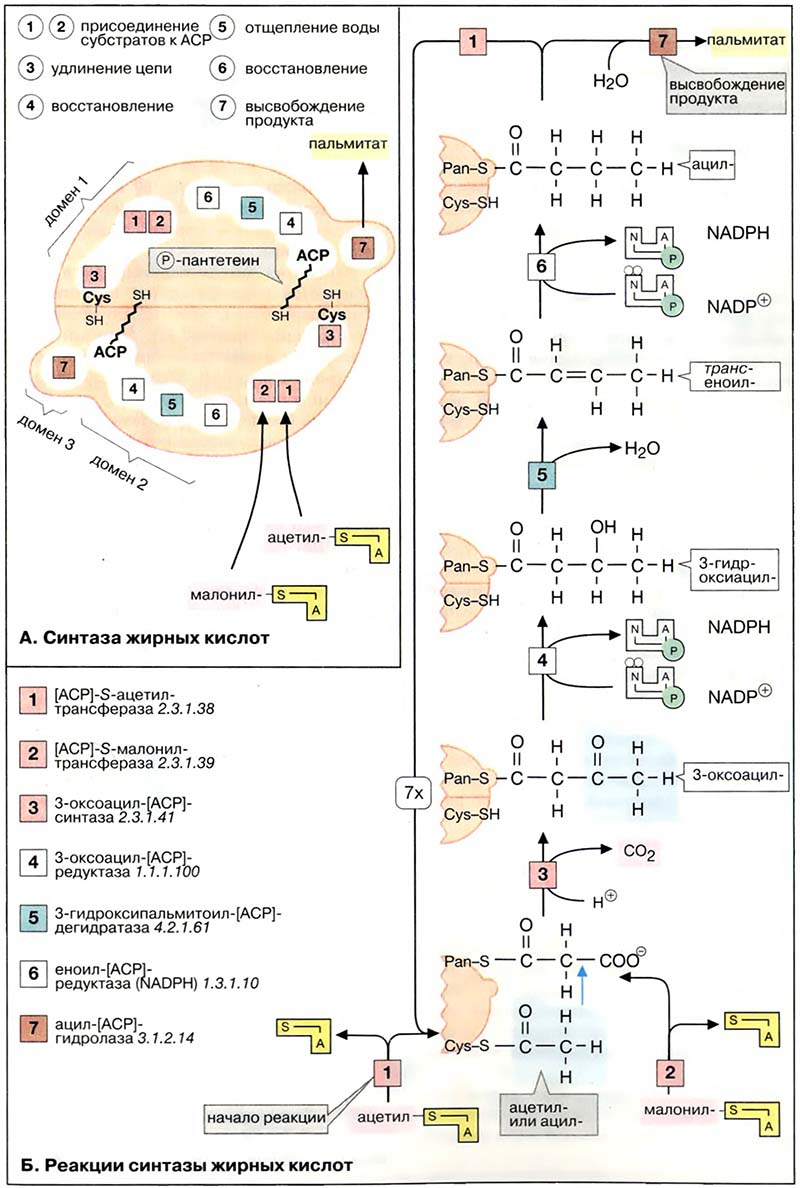
Каждая половинка синтазы жирных кислот может связывать субстрат тиолсложно-эфирной связью (ацильный или ацетильный остаток) по двум SH-группам: цистеинового остатка (Cys-SH) и 4′-фосфопантетеиновой группы (Pan-SH). Pan-SH, очень похожий на кофермент А (см. Коферменты переноса групп), связан с доменом синтазы, который называют ацилпереносящим белком [АПБ (АСР)]. Эта часть фермента функционирует как «длинная рука», которая фиксирует субстрат и передаёт его от одного реакционного центра к другому. Интересно отметить, что реакция при этом зависит от согласованности действия обеих половинок синтазы. Поэтому фермент функционально активен только в виде димера.
Активность мультиферментного комплекса пространственно распределена по трём различным доменам. Домен 1 катализирует перенос субстратов ацетил-КоА и малонил-КоА [АПБ]-S-ацетилтрансферазой [1] и [АПБ]-S-малонилтрансферазой [2] и последующую конденсацию обоих партнёров 3-оксоацил-[АПБ]-синтазой [3], домен 2 восстанавливает растущую цепь жирной кислоты с помощью 3-оксоацил-[АПБ]-редуктазы [4], 3-гидроксиацил-[АПБ]-дегидратазы [5] и еноил-[АПБ]-редуктазы [6]. Наконец, домен 3 после семи циклов удлинения цепи катализирует высвобождение готового продукта с помощью ацил-[АПБ]-гидролазы [7].
Каждая половинка синтазы жирных кислот может связывать субстрат тиолсложно-эфирной связью (ацильный или ацетильный остаток) по двум SH-группам: цистеинового остатка (Cys-SH) и 4′-фосфопантетеиновой группы (Pan-SH). Pan-SH, очень похожий на кофермент А (см. Коферменты переноса групп), связан с доменом синтазы, который называют ацилпереносящим белком [АПБ (АСР)]. Эта часть фермента функционирует как «длинная рука», которая фиксирует субстрат и передаёт его от одного реакционного центра к другому. Интересно отметить, что реакция при этом зависит от согласованности действия обеих половинок синтазы. Поэтому фермент функционально активен только в виде димера.
Активность мультиферментного комплекса пространственно распределена по трём различным доменам. Домен 1 катализирует перенос субстратов ацетил-КоА и малонил-КоА [АПБ]-S-ацетилтрансферазой [1] и [АПБ]-S-малонилтрансферазой [2] и последующую конденсацию обоих партнёров 3-оксоацил-[АПБ]-синтазой [3], домен 2 восстанавливает растущую цепь жирной кислоты с помощью 3-оксоацил-[АПБ]-редуктазы [4], 3-гидроксиацил-[АПБ]-дегидратазы [5] и еноил-[АПБ]-редуктазы [6]. Наконец, домен 3 после семи циклов удлинения цепи катализирует высвобождение готового продукта с помощью ацил-[АПБ]-гидролазы [7].
Статьи раздела «Биосинтез жирных кислот»:
- Биосинтез жирных кислот
- А. Синтаза жирных кислот
- Б. Реакции синтазы жирных кислот
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Лекции по природоведческой микробиологии
Лекции по природоведческой микробиологии Книга основана на курсе лекций, прочитанных в МГУ им. М. В. Ломоносова в 1995-2002 гг. ...
В монографии рассматривается история развития учения об «антропотоксинах», ...
 Koneman’s Color Atlas and Textbook of Diagnostic Microbiology
Koneman’s Color Atlas and Textbook of Diagnostic Microbiology Long considered the definitive work in its field, this new edition presents all the principles and practices readers need for a solid grounding in all ...
Учебное пособие, в котором авторы из США и Великобритании в доступной форме ...