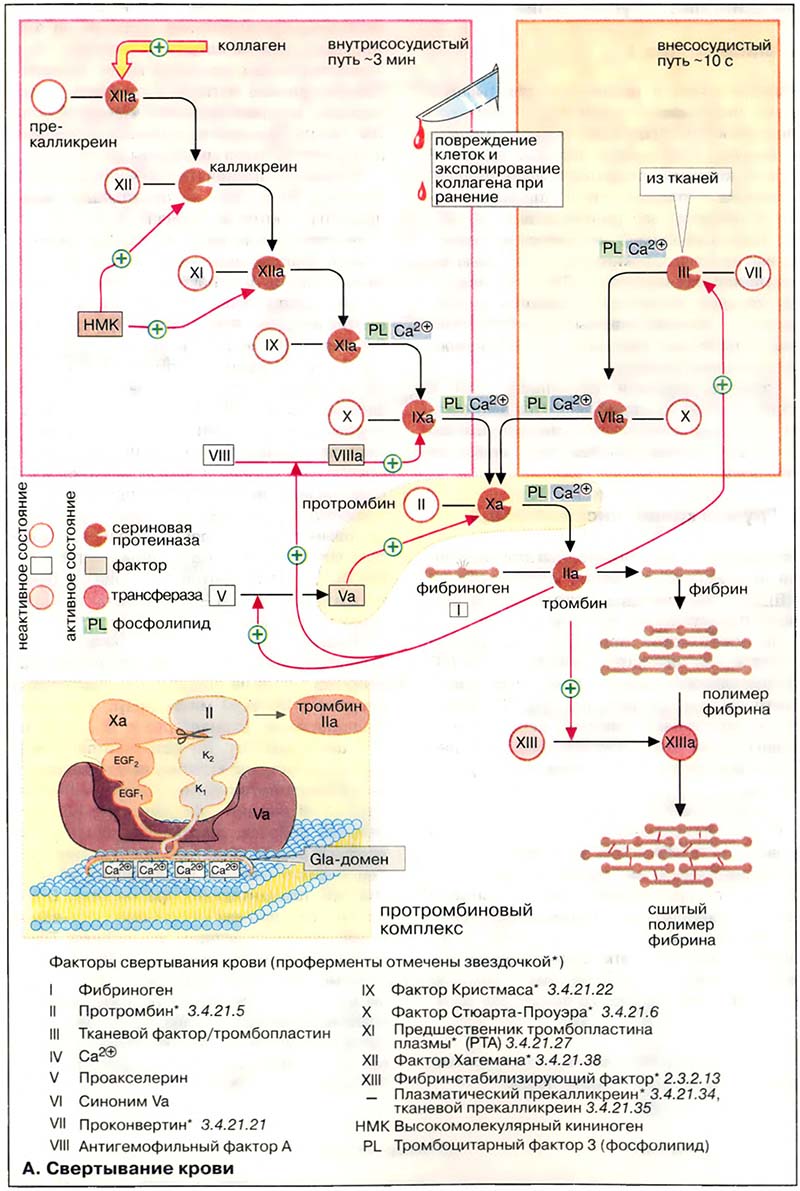
При свёртывании крови происходит ферментативное превращение растворимого белка плазмы фибриногена (фактора I. см. Дыхание и брожение) в фибриновый полимер, сеть волокон нерастворимого белка. В этой реакции принимает участие фермент тромбин (фактор IIа), который протеолитически отщепляет от молекулы фибриногена небольшой пептидный фрагмент, в результате чего освобождаются участки связывания, что позволяет молекуле фибрина агрегировать в полимер. Затем с помощью глутамин-трансферазы (фактора XIII) образуются изопептидные связи боковых цепей аминокислот фибрина, что приводит к формированию нерастворимого фибринового сгустка (тромба).
Свёртывание крови может запускаться двумя различными путями: вследствие нарушения целостности ткани (внесосудистый путь, на схеме справа) или процессами, которые начинаются на внутренней поверхности сосуда (внутрисосудистый путь, на схеме слева). В обоих случаях запускается каскад протеолитических реакций: из неактивных предшественников ферментов (зимогенов, условно обозначаемых на схеме окружностями) путём отщепления пептидов образуются активные сериновые протеиназы (обозначаемые на схеме окрашенными кружочками с вырезанным сектором), которые в свою очередь действуют на другие белки. Оба реакционных пути нуждаются в ионах Ca2+ и фосфолипидах [ФЛ (PL)] и оба завершаются активацией фактором Xa протромбина (фактора II) с образованием тромбина (IIа).
Внутрисосудистый путь инициируется коллагеном, который в норме не экспонирован на внутренней поверхности кровеносных сосудов: его контакт с кровью приводит к активации фактора XII. Внесосудистый путь активации начинается с освобождения фактора III (тканевого тромбопластина) из повреждённых клеток ткани. В течение нескольких секунд этот фактор приводит к свёртыванию крови в области раны.
Факторы свёртывания II, VII, IX и X содержат необычную аминокислоту, γ-карбоксиг-лутаминовую (Gla). Остатки Gla, которые образуются в результате посттрансляционного карбоксилирования остатков глутаминовой кислоты, группируются в особых белковых доменах. Они присоединяют ионы Ca2+ и вследствие этого связывают соответствующие регуляторные факторы с фосфолипидами на поверхности плазматической мембраны. На рисунке это схематически представлено на примере протромбинового комплекса (Va, Xa и II). Вещества, способные связывать свободные ионы Ca2+ в виде комплекса, например цитрат, предотвращают это взаимодействие с фосфолипидами и тормозят свёртывание. Для синтеза остатков Gla необходим в качестве кофактора витамин K (см. Медиаторы нервной системы). Антагонисты витамина К, такие, как дикумарин, подавляют синтез активных факторов коагуляции и действуют поэтому также как ингибиторы свёртывания.
Генетически обусловленный дефицит отдельных факторов свёртывания приводит к кровоточивости (гемофилия).
Контроль за свёртыванием крови (не показан на схеме). Процесс свёртывания крови находится в постоянном равновесии между активацией и торможением. Для торможения в плазме имеются очень эффективные ингибиторы протеиназ. Сериновые протеиназы системы свёртывания инактивируются антитромбином. Его действие усиливается сульфатированным глюкозаминогликаном — гепарином (см. Состав межклеточного матрикса). Тромбомодулин, расположенный на внутренней стенке кровеносных сосудов, инактивирует тромбин, образуя с ним стехиометрический комплекс. За протеолитическое разрушение факторов V и VIII в плазме отвечает белок c. Этот белок в свою очередь активируется тромбином и, тем самым, реализуется самотормозящийся механизм свёртывания крови.
Свёртывание крови может запускаться двумя различными путями: вследствие нарушения целостности ткани (внесосудистый путь, на схеме справа) или процессами, которые начинаются на внутренней поверхности сосуда (внутрисосудистый путь, на схеме слева). В обоих случаях запускается каскад протеолитических реакций: из неактивных предшественников ферментов (зимогенов, условно обозначаемых на схеме окружностями) путём отщепления пептидов образуются активные сериновые протеиназы (обозначаемые на схеме окрашенными кружочками с вырезанным сектором), которые в свою очередь действуют на другие белки. Оба реакционных пути нуждаются в ионах Ca2+ и фосфолипидах [ФЛ (PL)] и оба завершаются активацией фактором Xa протромбина (фактора II) с образованием тромбина (IIа).
Внутрисосудистый путь инициируется коллагеном, который в норме не экспонирован на внутренней поверхности кровеносных сосудов: его контакт с кровью приводит к активации фактора XII. Внесосудистый путь активации начинается с освобождения фактора III (тканевого тромбопластина) из повреждённых клеток ткани. В течение нескольких секунд этот фактор приводит к свёртыванию крови в области раны.
Факторы свёртывания II, VII, IX и X содержат необычную аминокислоту, γ-карбоксиг-лутаминовую (Gla). Остатки Gla, которые образуются в результате посттрансляционного карбоксилирования остатков глутаминовой кислоты, группируются в особых белковых доменах. Они присоединяют ионы Ca2+ и вследствие этого связывают соответствующие регуляторные факторы с фосфолипидами на поверхности плазматической мембраны. На рисунке это схематически представлено на примере протромбинового комплекса (Va, Xa и II). Вещества, способные связывать свободные ионы Ca2+ в виде комплекса, например цитрат, предотвращают это взаимодействие с фосфолипидами и тормозят свёртывание. Для синтеза остатков Gla необходим в качестве кофактора витамин K (см. Медиаторы нервной системы). Антагонисты витамина К, такие, как дикумарин, подавляют синтез активных факторов коагуляции и действуют поэтому также как ингибиторы свёртывания.
Генетически обусловленный дефицит отдельных факторов свёртывания приводит к кровоточивости (гемофилия).
Контроль за свёртыванием крови (не показан на схеме). Процесс свёртывания крови находится в постоянном равновесии между активацией и торможением. Для торможения в плазме имеются очень эффективные ингибиторы протеиназ. Сериновые протеиназы системы свёртывания инактивируются антитромбином. Его действие усиливается сульфатированным глюкозаминогликаном — гепарином (см. Состав межклеточного матрикса). Тромбомодулин, расположенный на внутренней стенке кровеносных сосудов, инактивирует тромбин, образуя с ним стехиометрический комплекс. За протеолитическое разрушение факторов V и VIII в плазме отвечает белок c. Этот белок в свою очередь активируется тромбином и, тем самым, реализуется самотормозящийся механизм свёртывания крови.
Статьи раздела «Свёртывание крови»:
- Свёртывание крови
- А. Свёртывание крови
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Микроэлементы в окружающей среде. Биогеохимия, биотехнология и биоремедиация
Микроэлементы в окружающей среде. Биогеохимия, биотехнология и биоремедиация Книга посвящена анализу роли микроэлементов (металлов и металлоидов) в ...
 Молекулярные аспекты жизни
Молекулярные аспекты жизни Два известных американских биохимика в сравнительно небольшой книге подвели ...
 NMR Studies of Structural Motifs: Protein Folding and Ligand Binding
NMR Studies of Structural Motifs: Protein Folding and Ligand Binding NMR of Structural Motifs: The agrin G3 domain is critical in development and maintenance of the neuromuscular junction. G3 binds -dystroglycan and ...
 Нелинейная динамика взаимодействующих популяций
Нелинейная динамика взаимодействующих популяций Проведён анализ режимов динамического поведения в системах нескольких ...