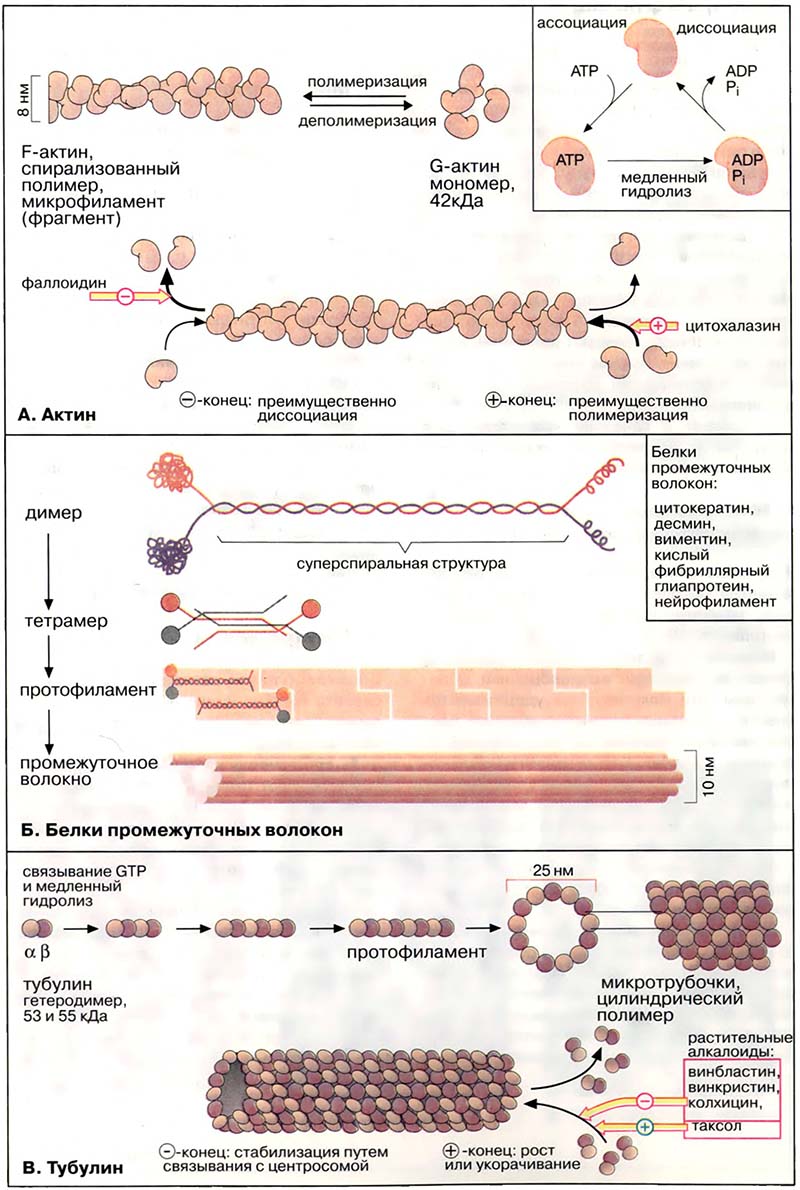
Микрофиламенты (актиновые нити) состоят из актина — белка, наиболее распространённого в эукариотических клетках. Актин может существовать в виде мономера (G-актин, «глобулярный актин») или полимера (F-актин, «фибриллярный актин»). G-актин — асимметричный глобулярный белок (42 кДа), состоящий из двух доменов. По мере повышения ионной силы G-актин обратимо агрегирует, образуя линейный скрученный в спираль полимер, F-актин. Молекула G-актина несёт прочно связанную молекулу АТФ (АТР), которая при переходе в F-актин, медленно гидролизуется до АДФ (ADP), то есть F-актин проявляет свойства АТФ-азы.
При полимеризации G-актина в F-актин ориентация всех мономеров одинакова, поэтому F-актин обладает полярностью. Волокна F-актина имеют два разноимённо заряженных конца — (+) и (-), которые полимеризуются с различной скоростью. Эти концы не стабилизированы специальными белками (как, например, в мышечных клетках), и при критической концентрации G-актина (+)-конец будет удлиняться, а (-)-конец укорачиваться. В условиях эксперимента этот процесс может быть ингибирован токсинами грибов. Например, фаллоидин (яд бледной поганки) связывается с (-)-концом и ингибирует деполимеризацию, в то время как цитохалазин (токсин из плесневых грибов, обладающий свойством цитостатика) присоединяется к (+)-концу, блокируя полимеризацию.
Актинассоциированные белки. В цитоплазме клеток имеются более 50 различных типов белков, которые специфически взаимодействуют с G-актином и F-актином. Эти белки выполняют различные функции: регулируют объем G-актинового пула (профилин), оказывают влияние на скорость полимеризации G-актина (виллин), стабилизируют концы нитей F-актина (фрагин, β-актинин), сшивают филаменты друг с другом или с другими компонентами (как, например, виллин, α-актинин, спектрин, MARCKS) или разрушают двойную спираль F-актина (гельзолин). Активность этих белков регулируется ионами Ca2+ и протеинкиназами.
При полимеризации G-актина в F-актин ориентация всех мономеров одинакова, поэтому F-актин обладает полярностью. Волокна F-актина имеют два разноимённо заряженных конца — (+) и (-), которые полимеризуются с различной скоростью. Эти концы не стабилизированы специальными белками (как, например, в мышечных клетках), и при критической концентрации G-актина (+)-конец будет удлиняться, а (-)-конец укорачиваться. В условиях эксперимента этот процесс может быть ингибирован токсинами грибов. Например, фаллоидин (яд бледной поганки) связывается с (-)-концом и ингибирует деполимеризацию, в то время как цитохалазин (токсин из плесневых грибов, обладающий свойством цитостатика) присоединяется к (+)-концу, блокируя полимеризацию.
Актинассоциированные белки. В цитоплазме клеток имеются более 50 различных типов белков, которые специфически взаимодействуют с G-актином и F-актином. Эти белки выполняют различные функции: регулируют объем G-актинового пула (профилин), оказывают влияние на скорость полимеризации G-актина (виллин), стабилизируют концы нитей F-актина (фрагин, β-актинин), сшивают филаменты друг с другом или с другими компонентами (как, например, виллин, α-актинин, спектрин, MARCKS) или разрушают двойную спираль F-актина (гельзолин). Активность этих белков регулируется ионами Ca2+ и протеинкиназами.
Статьи раздела «Цитоскелет: состав»:
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Математические модели морфогенеза
Математические модели морфогенеза Автором предлагаемого курса лекций по математическим моделям морфогенеза ...
 Клеточные механизмы токсичности аммиака
Клеточные механизмы токсичности аммиака В настоящей книге авторы попытались кратко изложить исторически сложившиеся и ...
В книге даётся богатейший, хорошо систематизированный справочный материал по ...
 Practical Forensic Microscopy: A Laboratory Manual
Practical Forensic Microscopy: A Laboratory Manual Forensic Microscopy: A Laboratory Manual will provide the student with a practical overview and understanding of the various microscopes and ...