Все дегидрогеназы нуждаются в коферменте для переноса восстановительных эквивалентов (см. Устройство и функционирование эндоплазматического ретикулума и аппарата Гольджи). Наиболее широко распространены коферменты динуклеотидного типа (см. Трансаминирование и дезаминирование), в котором два нуклеозид-5′-монофосфата соединены фосфоангидридной связью. ЛДГ и многие другие дегидрогеназы нуждаются в никотинамидаденин-динуклеотиде, сокращённо НАД+ (NAD+) (1). Обе нуклеотидных группы НАД+ построены из 5′-АМФ и нуклеотида, содержащего в качестве основания амид никотиновой кислоты (см. Водорастворимые витамины. I). Структурно (но не функционально) похожим коферментом является НАДФ+ (NADP+), в котором 2′-OH-группы рибозы аденина дополнительно связаны с фосфатом. Несмотря на близкое структурное родство НАД+ и НАДФ+ осуществляют различные функции в обмене веществ (см. Геном).
В окислительно-восстановительных реакциях пиридиннуклеотидного кофермента участвует только никотинамидное кольцо (2). Никотинамид является амидом пиридин-3-карбоновой (никотиновой) кислоты. В окисленной форме кольцо имеет ароматический характер и несёт положительный заряд. По этой причине кофермент в окисленном состоянии обозначают как НАД+. При окислении лактата дегидрогеназа отщепляет от субстрата (AH2) два атома водорода [то есть два электрона и два протона (2, середина)]. Однако на НАД+ переносится только гидрид-ион (Н′′, два электрона и один протон). Акцептором гидрид-иона является атом углерода в пара-положении к атому азота кольца НАД+. В этом месте образуется алифатическая CH2-группа, перестраиваются двойные связи кольца и исчезает положительный заряд (2, внизу). При окислении или восстановлении никотинамидного кольца изменяются также спектральные характеристики кофермента. Поэтому за реакцией можно легко следить фотометрически (см. Ферментативный анализ).
Второй протон высвобождается в среду и, следовательно, правильное наименование восстановленной формы кофермента NADH + Н+, а не NADH2.
В окислительно-восстановительных реакциях пиридиннуклеотидного кофермента участвует только никотинамидное кольцо (2). Никотинамид является амидом пиридин-3-карбоновой (никотиновой) кислоты. В окисленной форме кольцо имеет ароматический характер и несёт положительный заряд. По этой причине кофермент в окисленном состоянии обозначают как НАД+. При окислении лактата дегидрогеназа отщепляет от субстрата (AH2) два атома водорода [то есть два электрона и два протона (2, середина)]. Однако на НАД+ переносится только гидрид-ион (Н′′, два электрона и один протон). Акцептором гидрид-иона является атом углерода в пара-положении к атому азота кольца НАД+. В этом месте образуется алифатическая CH2-группа, перестраиваются двойные связи кольца и исчезает положительный заряд (2, внизу). При окислении или восстановлении никотинамидного кольца изменяются также спектральные характеристики кофермента. Поэтому за реакцией можно легко следить фотометрически (см. Ферментативный анализ).
Второй протон высвобождается в среду и, следовательно, правильное наименование восстановленной формы кофермента NADH + Н+, а не NADH2.
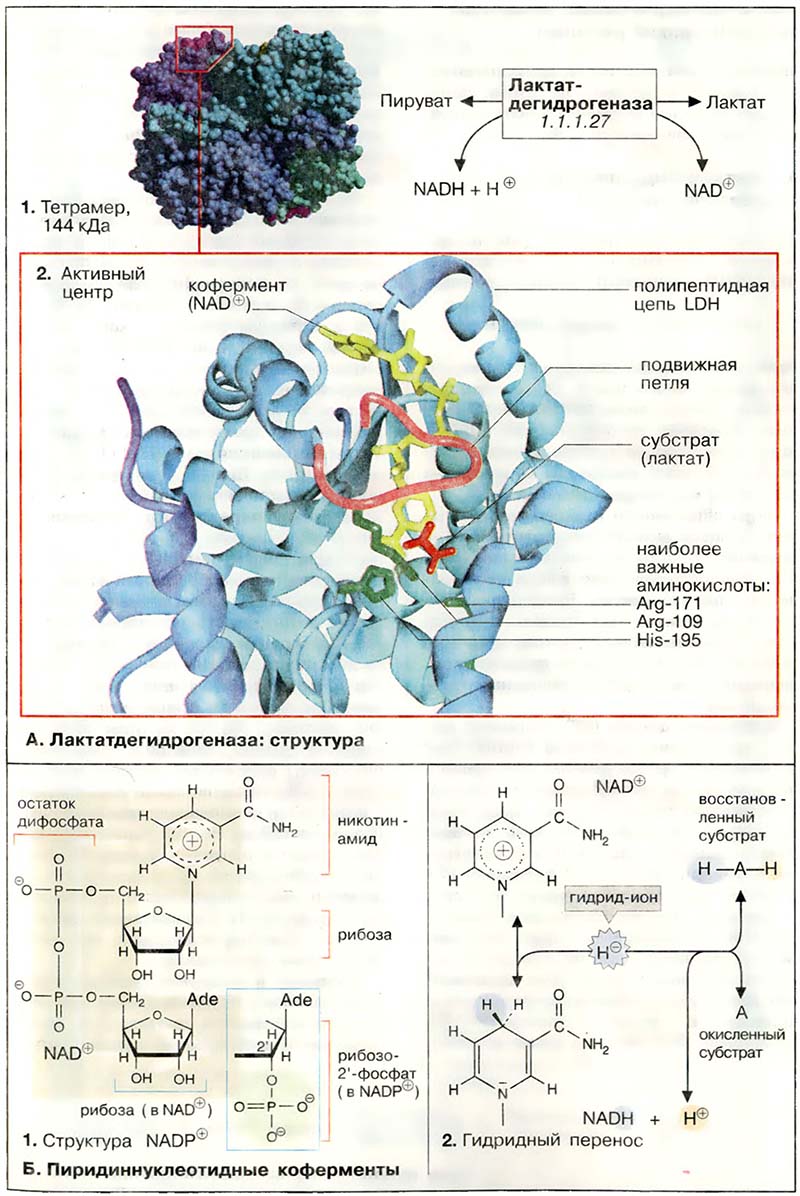
Статьи раздела «Лактатдегидрогеназа: структура»:
- Лактатдегидрогеназа: структура
- А. Лактатдегидрогеназа: структура
- Б. Пиридиннуклеотидные коферменты
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
As the title suggests, Isotope Effects in the Chemical, Geological and Bio Sciences deals with differences in the properties of isotopically ...
 Солитоны в молекулярных системах
Солитоны в молекулярных системах В монографии изложены новейшие подходы к изучению транспорта энергии и ...
 Объекты биологии развития
Объекты биологии развития Монография представляет собой вторую книгу из серии «Проблемы биологии ...
 Биохимия человека (комплект из 2 книг)
Биохимия человека (комплект из 2 книг) Настоящий учебник биологической и медицинской химии и молекулярной биологии ...