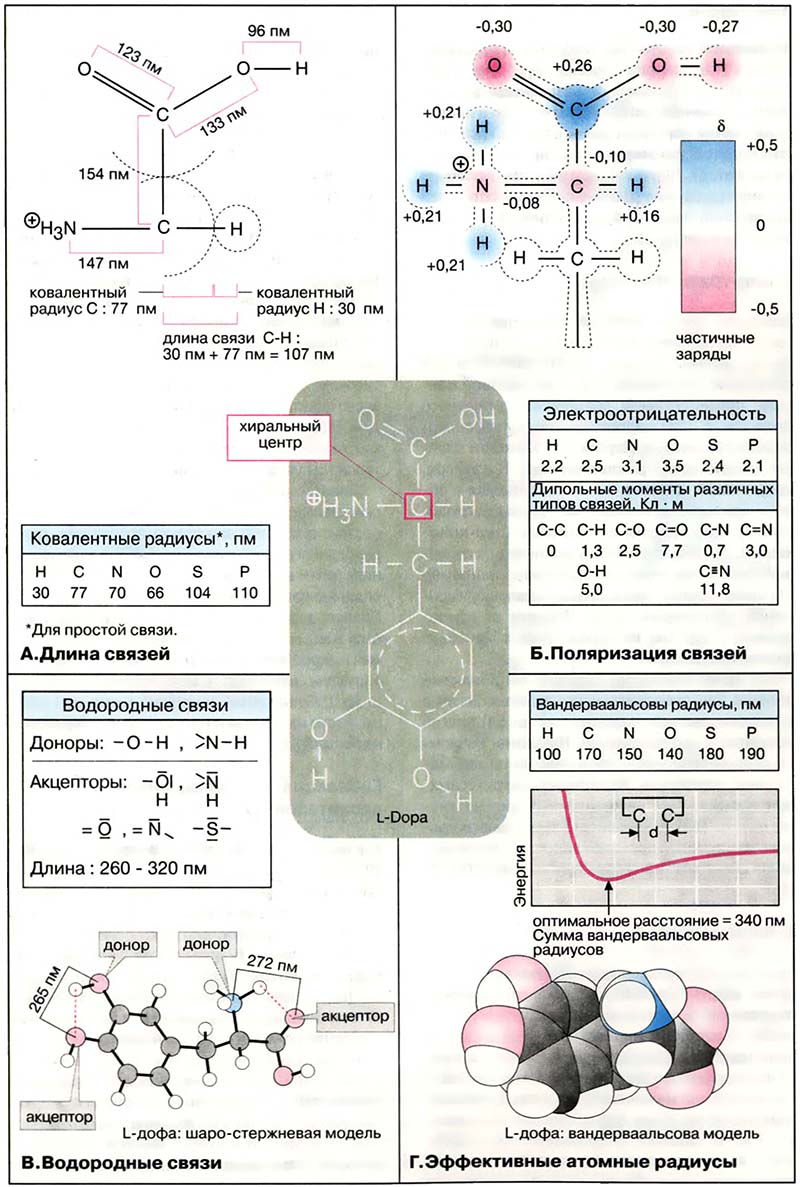
Особый тип нековалентной связи — водородная связь — имеет в биохимии исключительно важное значение. В образовании водородной связи принимают участие атомы водорода OH-, NH- и SH-групп (так называемых доноров водородной связи), которые взаимодействуют со свободной парой электронов атомов-акцепторов (например, O, N или S). Энергия водородной связи составляет 10-40 кДж/моль, что значительно меньше энергии ковалентной связи (меньше 400 кДж/моль). Однако многочисленные водородные связи вносят существенный вклад в стабилизацию структуры многих макромолекул (см. Глюконеогенез, Дезоксирибонуклеиновые кислоты). Например, L-дофа может образовывать две внутримолекулярные водородные связи. На шаро-стержневой модели L-дофа водородные мостики указаны штрихами.
Статьи раздела «Строение молекул»:
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Молекулярная и клеточная биология (комплект из 3 книг)
Молекулярная и клеточная биология (комплект из 3 книг) В книге известного учёного ФРГ на самом современном уровне обсуждены последние ...
 Physical Properties of Macromolecules
Physical Properties of Macromolecules Explains and analyzes polymer physical chemistry research methods and experimental data Taking a fresh approach to polymer physical chemistry, ...
