Положение редокс-пары в ряду определяется окислительно-восстановительным потенциалом. Последний определяют (см. Равновесие) с помощью электрохимической ячейки, которая позволяет оценивать перенос электронов между двумя редокс-парами, находящимися в разных сосудах. Прохождение электрического тока в результате переноса электронов между двумя химическими частицами, находящимися в разных сосудах, осуществляется через проводник, то есть химическая энергия трансформируется в электрическую.
В цепь встроен высокоомный вольтметр, исключающий прохождение электрического тока. Измеряют не ток, а электрическое напряжение, которое соответствует разности электрического потенциала ΔE двух растворов. Восстановительный потенциал системы определяется как э.д.с. в вольтах (В), измеренная против известного потенциала, возникающего в стандартном полуэлементе (полуячейке). В качестве стандарта принят восстановительный потенциал системы 2H+/H2 («водородный электрод»), который при определённых условиях условно считают равным нулю. Измеренный относительно стандарта потенциал конкретной окислительно-восстановительной пары может иметь знак плюс или знак минус. Величина Е зависит от концентрации реагентов и условий проведения реакции. Поэтому вводят понятие стандартный окислительно-восстановительный потенциал (или восстановительный потенциал Е°, поскольку он характеризует реакцию восстановления), который определяют как потенциал восстановления данной редокс-пары в стандартных условиях и при равных концентрациях всех реагентов, а также Е°’, определяемый как Е° при pH 7. Если пары расположить в порядке возрастания их восстановительных потенциалов, то получим электрохимический ряд напряжений (4). Спонтанный перенос электрона возможен лишь в том случае, если восстановительный потенциал вещества, которое должно отдавать электроны, — величина более отрицательная по сравнению с потенциалом вещества, которое должно принимать электроны.
В цепь встроен высокоомный вольтметр, исключающий прохождение электрического тока. Измеряют не ток, а электрическое напряжение, которое соответствует разности электрического потенциала ΔE двух растворов. Восстановительный потенциал системы определяется как э.д.с. в вольтах (В), измеренная против известного потенциала, возникающего в стандартном полуэлементе (полуячейке). В качестве стандарта принят восстановительный потенциал системы 2H+/H2 («водородный электрод»), который при определённых условиях условно считают равным нулю. Измеренный относительно стандарта потенциал конкретной окислительно-восстановительной пары может иметь знак плюс или знак минус. Величина Е зависит от концентрации реагентов и условий проведения реакции. Поэтому вводят понятие стандартный окислительно-восстановительный потенциал (или восстановительный потенциал Е°, поскольку он характеризует реакцию восстановления), который определяют как потенциал восстановления данной редокс-пары в стандартных условиях и при равных концентрациях всех реагентов, а также Е°’, определяемый как Е° при pH 7. Если пары расположить в порядке возрастания их восстановительных потенциалов, то получим электрохимический ряд напряжений (4). Спонтанный перенос электрона возможен лишь в том случае, если восстановительный потенциал вещества, которое должно отдавать электроны, — величина более отрицательная по сравнению с потенциалом вещества, которое должно принимать электроны.
Статьи раздела «Окислительно-восстановительные процессы»:
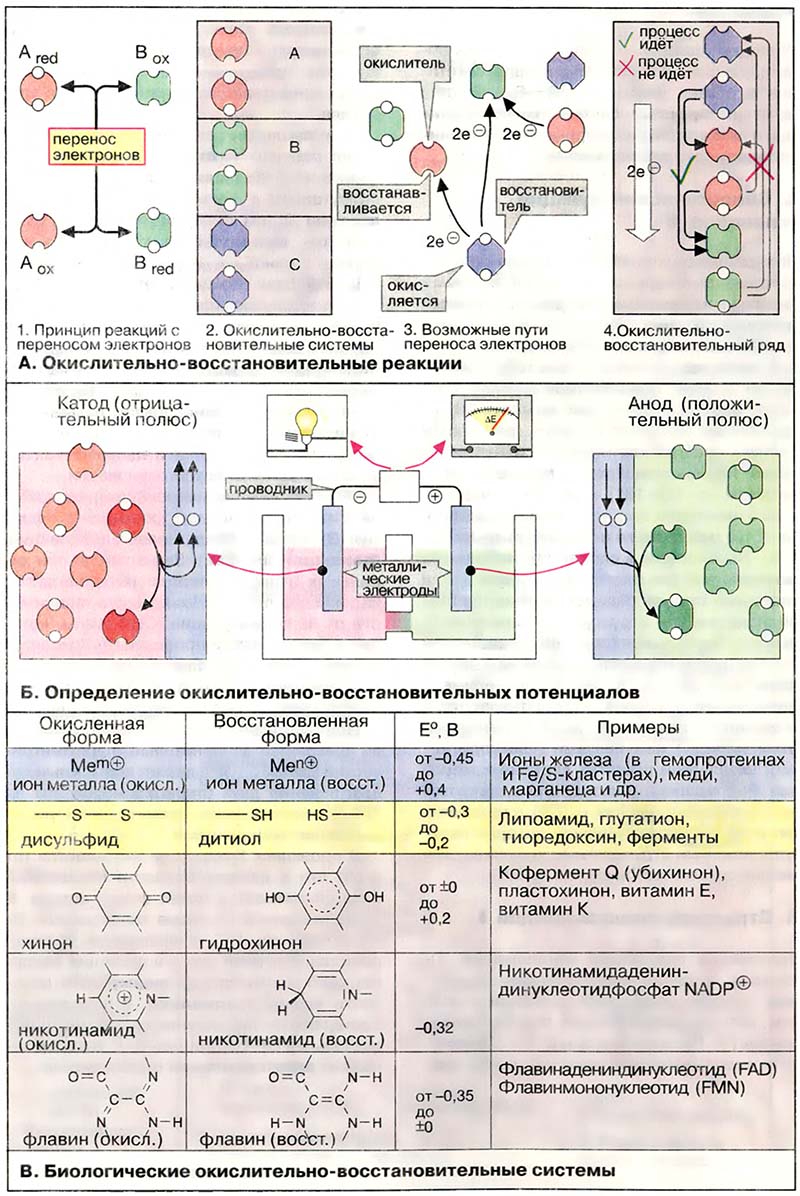
- А. Окислительно-восстановительные реакции
- Б. Определение окислительно-восстановительных потенциалов
- В. Биологические окислительно-восстановительные пары
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Открытие основных законов жизни
Открытие основных законов жизни В книге изложены история развития и основные достижения молекулярной биологии — ...
 Introductory Chemistry: Concepts and Critical Thinking (6th Edition)
Introductory Chemistry: Concepts and Critical Thinking (6th Edition) Introductory Chemistry: Concepts and Critical Thinking, Sixth Edition is a comprehensive learning system that offers print and media resources as well ...
