Структурные изменения, которые сопровождают взаимопревращения гликоген-фосфорилазы, были установлены рентгеноструктурным анализом. Фермент представляет собой димер с симметрией второго порядка. Каждая субъединица имеет активный центр, который расположен внутри белка и в b-форме плохо доступен для субстрата. Взаимопревращение начинается с фосфорилирования серинового остатка (Ser-14) вблизи N-конца каждой из субъединиц. С фосфатными группами связываются остатки аргинина соседних субъединиц. Связывание инициирует конформационные перестройки, которые существенно увеличивают сродство фермента к аллостерическому активатору АМФ. Действие АМФ и влияние кон-формационных изменений на активные центры приводят к возникновению более активной a-формы. После удаления фосфатных остатков фермент самопроизвольно принимает исходную b-конформацию.
Статьи раздела «Гормональный контроль»:
- Гормональный контроль
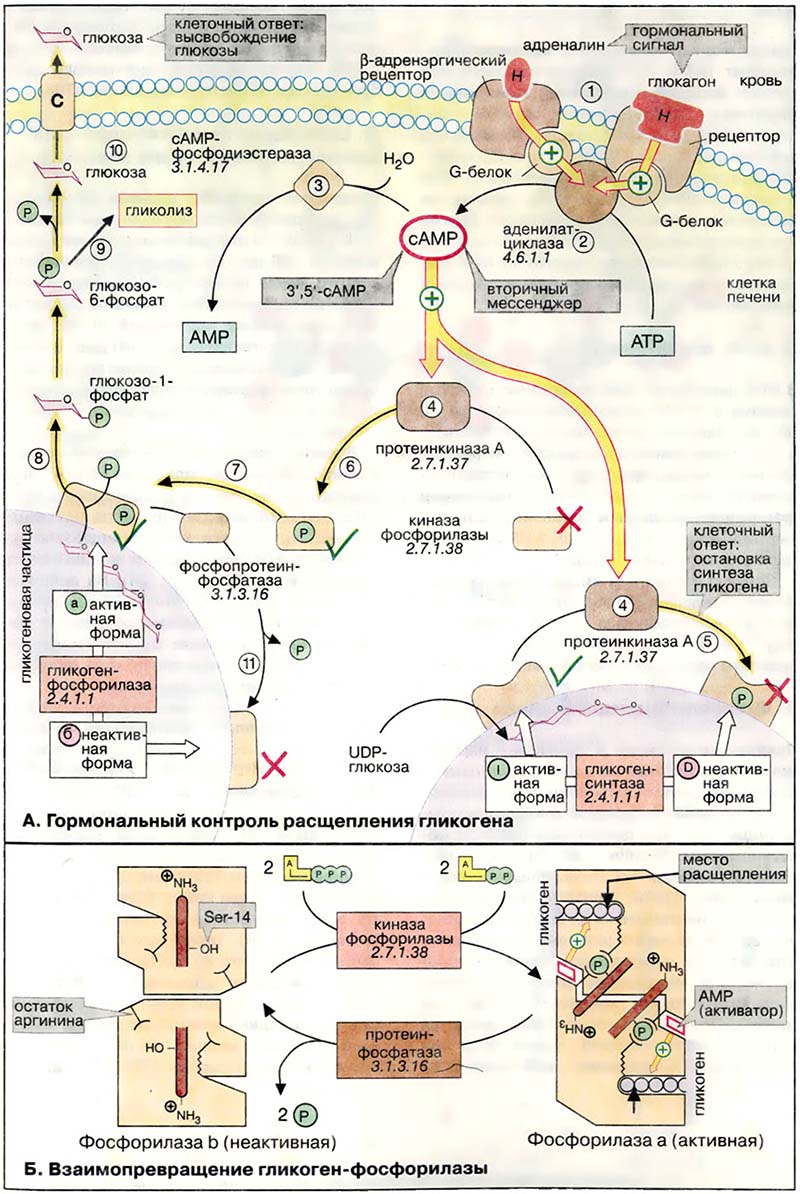
- А. Гормональный контроль расщепления гликогена
- Б. Взаимопревращение гликоген-фосфорилазы
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Geobiology: Objectives, Concepts, Perspectives, First Edition
Geobiology: Objectives, Concepts, Perspectives, First Edition Book DescriptionGeobiology is an exciting and rapidly developing research discipline that opens new perspectives in understanding Earth as a system. ...
 Introductory Chemistry: Concepts and Critical Thinking (6th Edition)
Introductory Chemistry: Concepts and Critical Thinking (6th Edition) Introductory Chemistry: Concepts and Critical Thinking, Sixth Edition is a comprehensive learning system that offers print and media resources as well ...
 Cell Biology: With STUDENT CONSULT Online Access
Cell Biology: With STUDENT CONSULT Online Access A masterful, richly illustrated introduction to the cell biology that you need to know.
 Fundamentals of Forensic DNA Typing
Fundamentals of Forensic DNA Typing An introductory text on forensic DNA analysis, written by the foremost expert in the field.