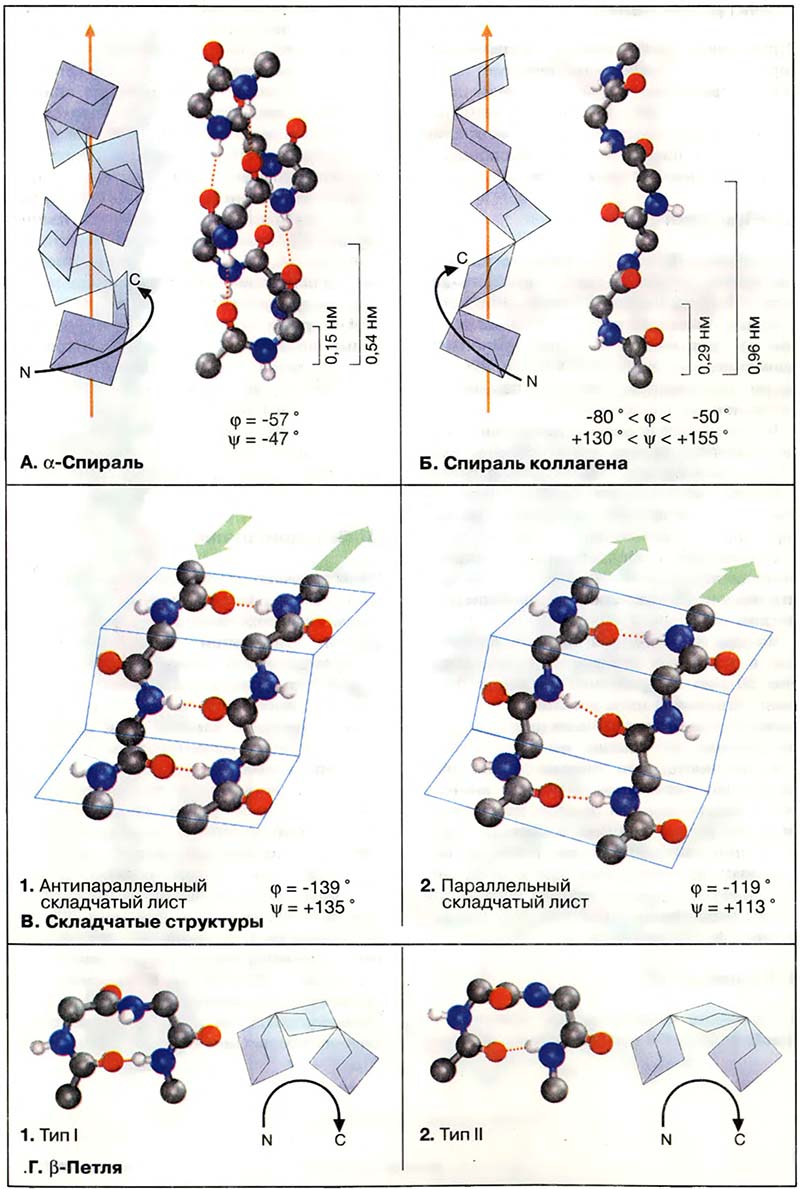
Наиболее распространённым элементом вторичной структуры является правая а-спираль (αR). Пептидная цепь здесь изгибается винтообразно (ось выделена оранжевым цветом). На каждый виток приходится 3,6 аминокислотного остатка, шаг винта (то есть минимальное расстояние между двумя эквивалентными точками) составляет 0,54 нм. α-Спираль стабилизирована почти линейными водородными связями (красный пунктир, см. Кислоты и основания) между NH-группой и CO-группой четвёртого по счету аминокислотного остатка. Таким образом, в протяжённых спиральных участках каждый аминокислотный остаток принимает участие в формировании двух водородных связей. Неполярные или амфифильные α-спирали с 5-6 витками часто обеспечивают заякоривание белков в биологических мембранах (трансмембранные спирали, см. Транспорт газов, Биомембраны: структура и функции).
Зеркально-симметричная относительно αR-спирали левая α-спираль (αL) встречается в природе крайне редко, хотя энергетически возможна.
Зеркально-симметричная относительно αR-спирали левая α-спираль (αL) встречается в природе крайне редко, хотя энергетически возможна.
Статьи раздела «Вторичные структуры белков»:
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Биофизическая химия. В 3 томах. Том 3
Биофизическая химия. В 3 томах. Том 3 В книге изложены представления о биологических макромолекулах и методах ...
 Cell Biology: With STUDENT CONSULT Online Access
Cell Biology: With STUDENT CONSULT Online Access A masterful, richly illustrated introduction to the cell biology that you need to know.
 Объекты биологии развития
Объекты биологии развития Монография представляет собой вторую книгу из серии «Проблемы биологии ...