Определённые сочетания двугранных углов φ и ψ (см. Гликолиз) встречаются в белках довольно часто. Если множество последовательно связанных аминокислотных остатков принимает стандартные конформации, формируются вторичные структуры, стабилизированные водородными мостиками в пределах одной пептидной цепи или между соседними цепями. Если такая регулярная структура распространяется на достаточно большой фрагмент молекулы белка, такой белок образует механически прочные нити или волокна. Подобного рода структурные белки (см. Структурные белки) имеют характерный аминокислотный состав.
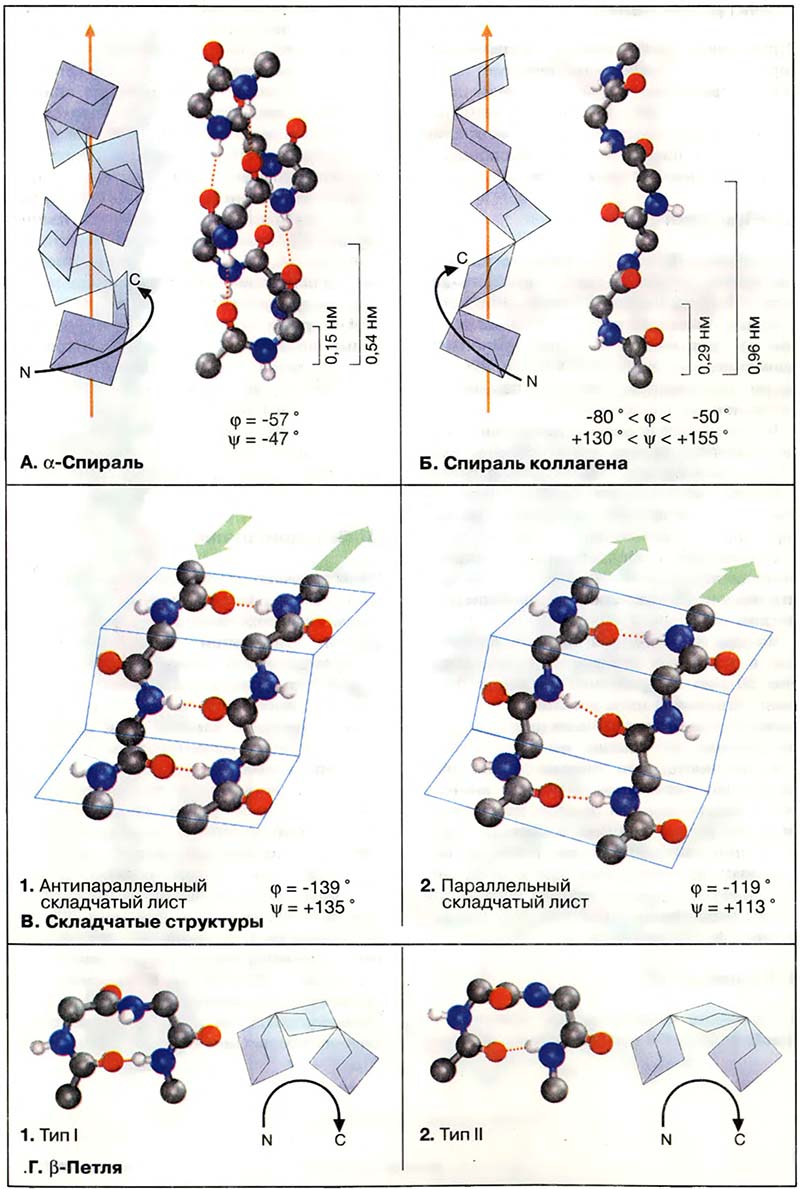
Здесь приведены основные элементы вторичных структур. На рисунках представлен остов полипептидной цепи, лишённый боковых цепей аминокислотных остатков. Для наглядности плоскости пептидных связей изображены в виде голубых пластин. Двугранные углы указанных структур приведены на конформационной карте Г1.
Здесь приведены основные элементы вторичных структур. На рисунках представлен остов полипептидной цепи, лишённый боковых цепей аминокислотных остатков. Для наглядности плоскости пептидных связей изображены в виде голубых пластин. Двугранные углы указанных структур приведены на конформационной карте Г1.
Статьи раздела «Вторичные структуры белков»:
- Вторичные структуры белков
- А. α-Спираль
- Б. Спираль коллагена
- В. Складчатые структуры
- Г. β-Петля
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
 Атлас. Морфология крахмала и крахмалопродуктов
Атлас. Морфология крахмала и крахмалопродуктов В атласе приведены данные о морфологической характеристике нативных крахмалов: ...
 Лекции по природоведческой микробиологии
Лекции по природоведческой микробиологии Книга основана на курсе лекций, прочитанных в МГУ им. М. В. Ломоносова в 1995-2002 гг. ...
 Биоматериалы, искусственные органы и инжиниринг тканей
Биоматериалы, искусственные органы и инжиниринг тканей Данная книга рассказывает о разработках, проводимых на стыке многих научных ...
Исследования, проводимые на микроорганизмах, внесли немалый вклад в изучение ...