Полный математический анализ ферментативной реакции приводит к сложным уравнениям, не пригодным для практического применения. Наиболее удобной оказалась простая модель, разработанная в 1913 году. Она объясняет характерную гиперболическую зависимость активности фермента от концентрации субстрата (1) и позволяет получать константы, которые количественно характеризуют эффективность фермента.
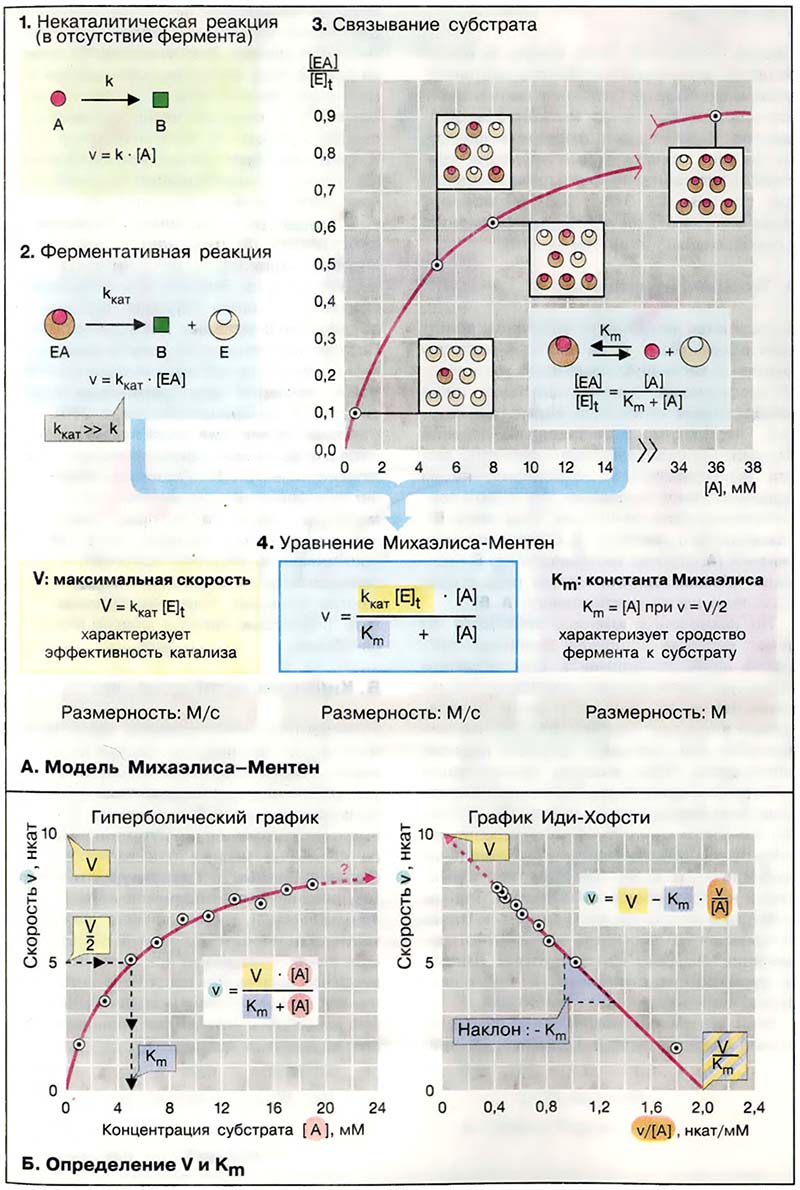
Модель Михаэлиса-Ментен исходит из того, что вначале субстрат A образует с ферментом Е (3) комплекс, который превращается в продукт B намного быстрее, чем в отсутствие фермента. Константа скорости kкат (2) намного выше, чем константа некаталитической реакции k. Константу kкат называют ещё «числом оборотов», поскольку она соответствует числу молекул субстрата, превращаемых в продукт одной молекулой фермента за 1 с. Согласно этой модели, активность фермента определяется долей комплекса ЕА от общей концентрации фермента [E]t, то есть, отношением [ЕА]/[E]t (3). С целью упрощения модель предполагает, что Е, A и ЕА находятся в химическом равновесии согласно закону действующих масс (см. Равновесие), что даёт в итоге для диссоциации комплекса ЕА уравнение:
[Е][А]/[ЕА] = Кm
Поскольку [E]t = [Е] + [ЕА],
[ЕА] = [E]t[A]/(Km + [А])
Из v = kкат[ЕА] (2) и предыдущего выражения получают уравнение Михаэлиса-Ментен (4).
Уравнение содержит две величины (два параметра), которые не зависят от концентрации субстрата [A], но характеризуют свойства фермента: это произведение kкат[Е]t соответствующее максимальной скорости реакции V при высокой концентрации субстрата, и константа Михаэлиса Km, характеризующая сродство фермента к субстрату. Константа Михаэлиса численно равна той концентрации субстрата [A], при которой v достигает половины максимальной величины V (если v = V/2, то [A]/(Km + [A]) = 1/2, то есть Km = [А]). Высокое сродство фермента к субстрату характеризуется низкой величиной Km и наоборот.
Модель Михаэлиса-Ментен основывается на нескольких не совсем реальных допущениях, таких, как необратимое превращение ЕА в Е + B, достижение равновесия между Е, A и ЕА, отсутствие в растворе других форм фермента, кроме Е и ЕА. Только при соблюдении этих гипотетических условий Km соответствует константе диссоциации комплекса, а kкат — константе скорости реакции ЕА → Е + B.
Модель Михаэлиса-Ментен исходит из того, что вначале субстрат A образует с ферментом Е (3) комплекс, который превращается в продукт B намного быстрее, чем в отсутствие фермента. Константа скорости kкат (2) намного выше, чем константа некаталитической реакции k. Константу kкат называют ещё «числом оборотов», поскольку она соответствует числу молекул субстрата, превращаемых в продукт одной молекулой фермента за 1 с. Согласно этой модели, активность фермента определяется долей комплекса ЕА от общей концентрации фермента [E]t, то есть, отношением [ЕА]/[E]t (3). С целью упрощения модель предполагает, что Е, A и ЕА находятся в химическом равновесии согласно закону действующих масс (см. Равновесие), что даёт в итоге для диссоциации комплекса ЕА уравнение:
[Е][А]/[ЕА] = Кm
Поскольку [E]t = [Е] + [ЕА],
[ЕА] = [E]t[A]/(Km + [А])
Из v = kкат[ЕА] (2) и предыдущего выражения получают уравнение Михаэлиса-Ментен (4).
Уравнение содержит две величины (два параметра), которые не зависят от концентрации субстрата [A], но характеризуют свойства фермента: это произведение kкат[Е]t соответствующее максимальной скорости реакции V при высокой концентрации субстрата, и константа Михаэлиса Km, характеризующая сродство фермента к субстрату. Константа Михаэлиса численно равна той концентрации субстрата [A], при которой v достигает половины максимальной величины V (если v = V/2, то [A]/(Km + [A]) = 1/2, то есть Km = [А]). Высокое сродство фермента к субстрату характеризуется низкой величиной Km и наоборот.
Модель Михаэлиса-Ментен основывается на нескольких не совсем реальных допущениях, таких, как необратимое превращение ЕА в Е + B, достижение равновесия между Е, A и ЕА, отсутствие в растворе других форм фермента, кроме Е и ЕА. Только при соблюдении этих гипотетических условий Km соответствует константе диссоциации комплекса, а kкат — константе скорости реакции ЕА → Е + B.
Статьи раздела «Кинетика ферментативных реакций»:
- Кинетика ферментативных реакций
- А. Модель Михаэлиса-Ментен
- Б. Определение V и Km
Структура:
Списки:
Сложность материала:
Величины и единицы:
Книги Список книг
Учебное пособие освещает систематизированную совокупность современных знаний ...
 Объекты биологии развития
Объекты биологии развития Монография представляет собой вторую книгу из серии «Проблемы биологии ...
 Солитоны в молекулярных системах
Солитоны в молекулярных системах В монографии изложены новейшие подходы к изучению транспорта энергии и ...
 Microbiology with Diseases by Taxonomy with MasteringMicrobiology (3rd Edition)
Microbiology with Diseases by Taxonomy with MasteringMicrobiology (3rd Edition) The Third Edition of Microbiology with Diseases by Taxonomy is the most cutting-edge microbiology book available, offering unparalleled currency, ...